| M. Ramharter, S. Winkler
Univ.-Klinik für Innere Medizin I, Klin. Abt. für
Infektionen und Chemotherapie, Medizinische Universität
Wien
(Leiter: Univ.-Prof. DDr. W. Graninger) |
|
Malaria
zählt weltweit zu den wichtigsten parasitären Erkrankungen
des Menschen, und ihre Bekämpfung stellt mehr denn je eine
globale Herausforderung dar. Trotz erfolgreicher Elimination
der Erkrankung aus einigen subtropischen Regionen der Welt sterben
heute mehr Menschen an Malaria als je zuvor. Die WHO schätzt
300 bis 500 Millionen Erkrankungsfälle und bis zu 3 Millionen
Todesfälle jährlich. Malaria-endemische Länder
gehören zu den ärmsten der Welt, wobei die Kombination
aus fehlenden Mitteln zur Kontrolle der Infektion und der enormen
Malaria-assoziierten ökonomischen Belastung dieser Länder
einen Teufelskreis mit hoher Erkrankungs-Prävalenz und
ausbleibender wirtschaftlicher Entwicklung bildet. |
| Geschichtliches
und Epidemiologie Die
Geschichte der Malaria ist vermutlich beinahe so alt wie die
Geschichte der Menschheit. Die Vorstellung über die Krankheit
und ihre Ursachen war in den verschiedenen Kulturen sehr unterschiedlich,
doch zeigen Namen wie Sumpffieber, Wechselfieber oder der aus
dem Italienischen stammende Begriff der „mal aria“
– der schlechten Luft also – schon frühe Vorstellungen
über die Entstehung, die Verbreitung und den Verlauf der
Erkrankung.
Lange
bevor der Malariaerreger 1880 durch den französischen Militärarzt
Alphonse Laveran entdeckt und die Übertragung auf den Menschen
durch den Stich der Anopheles-Mücke von Ronald Ross und
Battista Grassi beschrieben wurde, war schon die ursächliche
Behandlung des Malariafiebers
bekannt. Im Okzident war bereits im 17. Jahrhunderts die lebensrettende
Wirkung von Extrakten der Jesuitenborke nach der sagenumwobenen
Heilung der Condesa de Chinchon bekannt geworden. Ähnlich
war die fiebersenkende Wirkung von Artemisia annua – einer
Verwandten des heimischen Beifußgewächses –
in China bereits seit mehr als einem Jahrtausend bekannt. Bei
beiden Substanzen wurde erst durch die moderne Labormedizin
die Ursache für ihre antipyretische Wirkung aufgezeigt.
Diese ist, wie sich herausstellte, spezifisch durch die antiparasitäre
Wirkung gegen Malariaerreger begründet.
Die
Erforschung der Malaria und die Entdeckung von Wirkstoffen,
die zur Behandlung und Prophylaxe eingesetzt werden konnten,
hatten neben medizinischen aber auch weltpolitische Konsequenzen.
So wurden beispielsweise die zuvor für europäische
Siedler, Missionare und Armeen undurchdringlichen Regionen Afrikas
erst durch die Produktion großer Mengen Chinins auf indischen
und indonesischen Plantagen der Kolonialisierung und all ihrer
(negativen?) Folgen zugängig.
In der ersten Hälfte des 20. Jahrhunderts wurde nicht zuletzt
durch die militärstrategische Bedeutung des Chinins die
Forschung an synthetischen Alternativen vorangetrieben, die
schließlich zur Entwicklung des Chloroquins durch die
deutsche IG Farben geführt hatte. Darüber hinaus wurden
durch die Produktion von synthetischen Insektiziden wie DDT
Substanzen verfügbar, mit denen erstmals effektiv gegen
Moskitopopulationen vorgegangen werden konnte. Getragen durch
diesen Fortschritt wurde
von der Weltgesundheitsorganisation in den 50er Jahren des letzten
Jahrhunderts ein weltweites Programm zur Eradikation der Malaria
gestartet – gestützt auf die Vektorbekämpfung
durch DDT und die Chemotherapie der Malaria mittels Chloroquin.
Zu
Beginn des 20. Jahrhunderts war die Malaria auch in Europa von
den sumpfigen Ebenen Mittel- und Süditaliens bis in den
Norden bei St. Petersburg und Südengland weit verbreitet.
Durch ein Zusammenspiel von verbesserten Gesundheitseinrichtungen,
ökologischen Maßnahmen, wie Trockenlegung von Sümpfen
und Vektorbekämpfung, und effektiven Therapiemöglichkeiten
kam es zu beeindruckenden Erfolgen und die Malaria wurde aus
Europa, Nordamerika, Australien und Teilen Asiens verdrängt.
Nur der Einfluss auf den am schwersten betroffenen afrikanischen
Kontinent war von Beginn an begrenzt.
Der
Erfolg des Malariaeradikationsprogramms war aber nicht in allen
Regionen von Dauer und es mehrten sich Berichte über fehlende
Fortschritte oder sogar eine Verschlechterung der Situation.
Durch die zunehmende Resistenzentwicklung der Malariaerreger
gegen gebräuchliche Malariamedikamente kam es zu steigenden
Problemen in der Therapie und Prophylaxe. Durch die parallel
fortschreitende Entwicklung von Resistenzen der Anopheles-Mücke
gegen DDT und andere Insektizide kam es schließlich zum
vorzeitigen Ende des Eradikationsprogramms. Dieses Scheitern
führte zu einem verminderten Engagement der Industriestaaten
in der Bekämpfung von Tropenkrankheiten.
Durch die damit verbundene Abnahme an finanziellen Ressourcen
und nicht zuletzt durch sozioökonomisch und politisch turbulente
Zeiten in einer Vielzahl afrikanischer Gebiete kam es in weiterer
Folge zu einer Zunahme der Malariamorbidität und - mortalität
des am schwersten betroffenen Kontinents.
40% der Menschheit leben in endemischen Gebieten und sind daher
dem Risiko einer Malaria-Erkrankung direkt ausgesetzt. Etwa
90% der weltweiten Krankheits- und Todesfälle an Malaria
sind im Afrika südlich der Sahara zu beklagen. Und dort
sind es wiederum Kinder und Schwangere, die einem besonders
hohen Risiko ausgesetzt sind.
|
Übertragungszyklus
Es gibt vier humanpathogene Plasmodienspezies (Tabelle
1): Plasmodium falciparum, der Erreger der Malaria
tropica, Plasmodium vivax und Plasmodium ovale,
die die Malaria tertiana verursachen, sowie Plasmodium malariae,
der Erreger der Malaria quartana. Neben diesen zum Großteil
anthroponotischen Erregern gibt es auch vereinzelte Berichte
über menschliche Infektionen durch tierpathogene Malariaerreger.
Zyklus
Der Lebenszyklus der vier für den Menschen pathogenen Plasmodien
ist im Allgemeinen auf die Anopheles-Mücke
und den Menschen beschränkt. Der eigentliche Hauptwirt
der Parasiten ist die weibliche Anopheles-Mücke. Von dieser
werden beim Stich Sporozoiten (ein Entwicklungsstadium des Malariaerregers)
in die Blutbahn des Menschen freigesetzt, die in Hepatozyten
einwandern, um die Leberschizogonie zu beginnen. Dabei kommt
es zu einer Vermehrung der Plasmodien, die anschließend
frühestens 5 - 7 Tage nach dem Moskitostich in die Blutbahn
freigesetzt werden. Schließlich kommt es zu einem Befall
der Erythrozyten und einer Vermehrung in diesen (Blutschizogonie).
Im Zuge dieser Vermehrung kommt es zur Zerstörung von Erythrozyten
und einem weiteren Befall neuer Erythrozyten. Ein Teil der Plasmodien
entwickelt sich parallel dazu zu Geschlechtsformen, den so genannten
Gametozyten, die wiederum von Blut saugenden Anopheles-Mücken
aufgenommen werden und in der Darmwand des Mückenmagens
die sexuelle Vermehrung vollziehen. Letztlich kommt es wieder
zur Produktion von Sporozoiten, die die Speicheldrüsen
der Mücken befallen und so den Lebenszyklus der Malariaerreger
schließen.
Bemerkenswert
ist die Tatsache, dass Plasmodium vivax und Plasmodium
ovale so genannte Schlafformen oder Hypnozoiten in der
Leber entwickeln, die Monate oder manchmal auch Jahre nach Ende
der Erkrankung durch Reaktivierung zu einer neuerlichen
Episode der Malaria tertiana führen können. Dies kann
nur durch eine medikamentöse Therapie verhindert werden.
Ähnlich kann es bei Plasmodium malariae sogar
noch Jahrzehnte nach der durchgemachten Infektion zu einem Wiederauftreten
der Erkrankung kommen, wenngleich das Überdauern der Malariaerreger
hierbei nicht durch Hypnozoiten, sondern durch Blutformen verursacht
wird. Auch diese Rückfälle sind durch effektive Therapie
zu verhindern.
Neben
dem natürlichen Übertragungszyklus sei auch noch die
Möglichkeit der Transfusionsmalaria erwähnt, die bei
ungenügenden Vorsichtsmaßnahmen vor allem zur Übertragung
von Malaria quartana führen kann. Auch kann es in Einzelfällen
durch Verschleppen infektiöser Mücken in Flugzeugen
und anderen Transportmitteln zur Malariaübertragung in
nicht endemischen Gebieten kommen.
Tabelle 1: humanpathogene
Plasmodienspezies
|
4
humanpathogene Spezies |
„alte“ Bezeichnung |
Plasmodium
falciparum |
Malaria
tropica |
Plasmodium
vivax
Plasmodium ovale |
Malaria
tertiana |
Plasmodium
malariae |
Malaria
quartana |
|
|
| Klinische
Manifestation Die
Malariaerkrankung wird nach den Erregern und dem klinischen
Verlauf in drei Formen unterteilt: Die Malaria tropica, die
durch Plasmodium falciparum verursacht wird und für
den weitaus größten Teil der Mortalität verantwortlich
ist, sowie die nur in Ausnahmefällen letal verlaufenden
Formen der Malaria tertiana (Plasmodium vivax und Plasmodium
ovale) und Malaria quartana (Plasmodium malariae).
Malaria
tropica
Der klinische Verlauf der Malaria tropica wird in asymptomatische
Infektionen, die praktisch ausschließlich bei semi-immunen
Bewohnern endemischer Gebiete auftreten, sowie unkomplizierte
und komplizierte Formen unterteilt. Obwohl der Übergang
notwendigerweise fließend ist, ist diese Unterscheidung
von prognostischer Bedeutung und damit auch von therapeutischer
Konsequenz. Vereinfacht dargestellt sind unkomplizierte Fälle
frühzeitig erkannte Infektionen, die bei prompter adäquater
Therapie eine gute Prognose aufweisen. Dem gegenüber stehen
komplizierte Fälle, die zumeist länger dauernde Infektionen
darstellen und eine zunehmend schlechtere Prognose aufweisen.
Unkomplizierte
Malaria tropica
Die häufigsten Symptome der unkomplizierten Malaria sind
Fieber, Kopfweh, Muskelschmerzen, Gelenkschmerzen, Augenschmerzen,
Durchfall, Schüttelfrost, Schwitzen, Antriebslosigkeit,
Appetitlosigkeit usw. Auch wenn Fieber zumeist ein führendes
Symptom darstellt, ist wichtig festzuhalten, dass keines der
oben genannten Symptome notwendigerweise vorhanden sein muss
und dass die klinische Diagnose durch die Vielzahl an verschiedenartigen
Symptomen erschwert wird. Untypische Verläufe sind das
eigentlich Typische an der Malaria tropica.
Komplizierte
Malaria tropica
Bei Fortschreiten der Malariaerkrankung kann es zur Entwicklung
einer komplizierten Malaria kommen. Es gibt eine Vielzahl an
Symptomen und Laborparametern, die von prognostischer Bedeutung
sind und in unterschiedlichen Klassifikationen Eingang finden.
Klinisch sind besonders der neurologische Zustand, das Auftreten
von Konvulsionen, respiratorischer Insuffizienz, Kreislaufkollaps,
Lungenödem, Blutungsneigung, Ikterus, Hämoglobinurie
und schwerer Anämie bedeutend. Bei massiver Beeinträchtigung
des Bewusstseins bis zum unweckbaren Koma spricht man auch von
zerebraler Malaria, während man bei besonders ausgeprägter
Anämie von schweren anämischen Verlaufsformen spricht.
Die Entwicklung der vorherrschenden Symptomatik ist vor allem
vom Alter, der spezifischen Immunitätslage des Patienten
und in weiterer Folge der epidemiologischen
Situation abhängig. Parasitäre Faktoren spielen vermutlich
ebenso eine Rolle, wie beim Verlauf der Schwangerschafts-assoziierten
Malaria gezeigt wurde. Zur prognostischen Bewertung des individuellen
Patienten sind die Bestimmung von Hämoglobin, Parasitämie,
Vorhandensein von Blutschizonten, Laktat und Glukosespiegel,
Säure-Basen-Status, und des Anteils an pigmentierten mononukleären
Zellen von Bedeutung. Bei Vorliegen einer komplizierten Malaria
ist der Patient so schnell wie möglich an eine Institution
mit der Möglichkeit der intensiv-medizinischen Betreuung
zu transferieren.
Malaria tertiana und Malaria quartana
Das klinische Bild der Malaria tertiana entspricht am ehesten
der klassischen Vorstellung des Wechselfiebers. Dabei kommt
es zu plötzlichem Anfiebern mit starkem Schüttelfrost
und anschließendem Abfiebern bei starkem Schwitzen. Typischerweise
liegt ein fieberfreier Tag zwischen zwei Fieberschüben.
Dieser typische Rhythmus war namensgebend für die Malaria
tertiana (Fieber am ersten und am dritten Tag). Obwohl die subjektive
Symptomatik der Malaria tertiana häufig stärker ausgeprägt
ist als bei der gefährlicheren Malaria tropica, verläuft
doch die überwiegende Mehrzahl der Erkrankungen gutartig.
Auch unbehandelt kommt es nach einigen Monaten zum Sistieren
der Symptome. Ohne medikamentöse Behandlung der in der
Leber befindlichen Hypnozoiten kann es aber noch nach Wochen
und Monaten zu immer wiederkehrenden Fieberepisoden kommen.
Bei
der Malaria quartana handelt es sich um ein ähnliches Erkrankungsbild
wie bei der Malaria tertiana. Unterschiedlich sind die zweitägige
Latenzphase zwischen Fieberschüben (daher der Name Quartana:
Fieber am ersten und vierten Tag) und das Fehlen
von Hypnozoiten in der Leber. Auch wenn die Malaria quartana
in aller Regel einen gutartigen Verlauf nimmt, kann es durch
die Entwicklung einer Glomerulonephritis zu mitunter tödlichem
Ausgang kommen. Darüber hinaus kann es natürlich auch
zu Mehrfachinfektionen kommen, bei denen ein Patient mit mehr
als nur einem Erreger infiziert ist. Dies ist zwar per se nicht
gefährlicher als die entsprechende Einzelinfektion, es
kann aber dadurch zu diagnostischen Schwierigkeiten und in weiterer
Folge zu inadäquaten Therapien kommen.
|
| Diagnose
Seit
der Entdeckung der Malariaerreger bis zum heutigen Tag ist der
direkte Erregernachweis im Mikroskop der Goldstandard der Malariadiagnostik.
Neben dem Blutausstrich, in dem die Morphologie der Malariaerreger
in den Erythrozyten am besten zu beurteilen ist, kommt dem so
genannten „Dicken Tropfen“ besondere Bedeutung zu.
Bei dieser Konzentrationsmethode kommt es durch das gleichzeitige
Betrachten einer Vielzahl von Blutschichten zu einer erhöhten
Sensitivität. Erst dadurch kann eine niedrige Parasitämie
mit einiger Sicherheit ausgeschlossen werden. Der Vorteil der
mikroskopischen Diagnostik besteht im niedrigen Preis, in der
Schnelligkeit der Diagnosestellung (nach etwa 30 Minuten sollte
ein endgültiges Ergebnis feststehen) und darin, dass nur
wenige Ressourcen dafür vorhanden sein müssen, sodass
diese Methode auch für ärmere Länder geeignet
ist. Weiters ist es die einzige praktikable Methode, um die
Parasitämie eines Patienten zu bestimmen, die aufgrund
ihres prognostischen Werts für die Wahl der Therapie mitentscheidend
ist. Nachteil dieser Methoden ist die Notwendigkeit der exzellenten
Schulung der Befunder, um verlässliche Ergebnisse zu gewährleisten.
Seit
einiger Zeit stehen auch immunchromatographische Tests für
die Diagnose der Malaria tropica und der Malaria tertiana zur
Verfügung. Vorteile dieser Tests sind die rasche und für
trainierte Hände unkomplizierte Testdurchführung,
die hohe Sensitivität für Malaria tropica und die
Durchführbarkeit ohne technische Hilfsmittel. Nachteile
sind vor allem die Tatsache, dass die Parasitämie nicht
bestimmt werden kann, die relativ zur Mikroskopie höheren
Kosten und die nur mäßige Verlässlichkeit der
Diagnose der Malaria tertiana. Außerdem kann mit diesen
Tests nicht mit Sicherheit über das eventuelle Vorhandensein
von Doppelinfektionen geurteilt werden. Weiters bleiben diese
Tests nach erfolgreicher Therapie einige Tage positiv und können
daher nicht zur Überwachung der Therapie eingesetzt werden.
Aufgrund dieser Eigenschaften sind die Kartentests auch für
den routinemäßigen Einsatz in endemischen Gebieten
nicht geeignet.
Die
PCR-Diagnostik ist vor allem von wissenschaftlichem Interesse,
da sie für den Patienten einerseits zu spät und andererseits
in den meisten endemischen Gebieten auch zu teuer kommen würde.
Außerdem sind quantifizierende PCR-Protokolle erst in
Entwicklung, mit denen auch die Parasitenlast bestimmt werden
könnte. Letztlich sind molekularbiologische Methoden derzeit
nur für immun-epidemiologische Fragestellungen und die
Identifikation von Resistenzgenen im Einsatz. Interessanterweise
können aufmerksame Labormediziner auch eine typische Streuung
der Monozytenpopulation in Hämatologieautomaten bei schweren
Malariainfektionen beobachten, die durch die Phagozytose des
Malariapigments verursacht wird. Der serologische Antikörpernachweis
hat hingegen bei der Diagnosestellung der akuten Erkrankung
keine Bedeutung und ist auch epidemiologisch nur von geringem
Wert.
|
| Therapie
Die
Therapie der Malaria tropica ist aufgrund ihres potenziell
letalen Verlaufs und der Entwicklung von Resistenzen gegenüber
Malariamedikamenten zunehmend komplizierter geworden. Die Chloroquin-Resistenz
von Plasmodium falciparum ist in so gut wie allen endemischen
Gebieten bereits so stark ausgebildet, dass andere Medikamente
zur Therapie herangezogen werden müssen. Zur oralen Therapie
stehen derzeit in Österreich Mefloquin (Lariam®) und
die Medikamentenkombinationen Atovaquone-Proguanil (Malarone®)
und Artemether-Lumefantrin (Riamet®; derzeit allerdings
in Österreich nicht mehr im Handel) zur Verfügung.
Auch wenn die Effektivität dieser Medikamente in etwa vergleichbar
ist, gibt es dennoch bedeutende Unterschiede in Bezug auf Wirkungsprofil
und Nebenwirkungen (Tabelle 2). Besonders
wichtig erscheint hier, dass die Diagnose der Erkrankung und
die prognostische Einteilung korrekt durchgeführt wird,
da es bei Übersehen von Risikofaktoren auch nach Therapiebeginn
zur Entwicklung einer mitunter letal verlaufenden komplizierten
Malaria tropica kommen kann.
Bei
komplizierter Malaria tropica zählt vor allem die Zeit.
Je schneller eine adäquate Therapie eingeleitet wird, umso
besser ist die Prognose. Derzeit ist in Österreich kein
einziges intravenöses Malaria-Medikament zugelassen, das
für die Therapie der komplizierten Malaria tropica routinemäßig
eingesetzt wird. Die Therapie der Wahl stellt die Verabreichung
von Chinin als Monotherapie oder in Kombination mit Doxycyclin
oder Clindamycin dar. Chinin kann in Form von Chinindihydrochlorid
über die internationale Apotheke bestellt werden. Besonderes
Augenmerk ist auf die Überwachung und Korrektur des Säure-Basen-Haushaltes
und der Blutglukosespiegel
zu legen. Da es durch Chinin zu kardialen Nebenwirkungen kommen
kann, ist außerdem ein kardiales Monitoring unerlässlich.
Desweiteren sind eine Flüssigkeitsbilanzierung und die
Messung des zentralen Venendrucks von Bedeutung, da es im Rahmen
einer komplizierten Malaria tropica häufig zur Ausbildung
eines oft letal verlaufenden Lungenödems kommen kann. Neben
der medikamentösen Therapie von Konvulsionen gibt es derzeit
keine adjuvante Therapie, die den Therapieerfolg positiv beeinflussen
würde.
Die
Therapie der Malaria tertiana und der Malaria quartana
ist vergleichsweise einfach. Bei Vorliegen einer Malaria tertiana
wird dem Patienten über drei Tage oral Chloroquin verabreicht.
Zur Vermeidung von Rückfällen, hervorgerufen durch
die Leberformen der Malaria tertiana, wird nach Ausschluss eines
erblichen Glukose-6-Phosphat-Dehydrogenase-Mangels über
14 Tage Primaquin eingenommen (ebenfalls in Österreich
nicht zugelassen). Aus einigen asiatischen Gebieten wurde die
Resistenz beziehungsweise verminderte Empfindlichkeit von Plasmodium
vivax gegen Chloroquin beschrieben. In diesen Fällen
sollte entweder Primaquin simultan mit Chloroquin eingenommen
werden oder statt Chloroquin ein neueres Medikament verschrieben
werden (zum Beispiel Malarone® oder Mefloquin®). Obwohl
in der wissenschaftlichen Literatur Berichte von letal verlaufenden
Plasmodium vivax-Infektionen aufscheinen (Milzruptur),
ist der Verlauf und die Prognose dennoch als sehr günstig
anzusehen.
Bei Vorliegen einer Malaria quartana-Infektion ist eine dreitägige
Chloroquin-Therapie bereits kurativ. Vorsicht ist allerdings
geboten, um keine Doppelinfektionen mit Plasmodium falciparum
zu übersehen.
Tabelle 2: Therapie der Malaria
| |
Substanzname |
Dosis |
Handelsname |
Dauer |
Kommentar |
| Malaria
tropica, unkompliziert |
| |
Atovaquone
+ Proguanil |
15
mg/kg + 6 mg/kg
(1 x tgl 4 Tabletten) |
Malarone |
Tag
1 - 3 |
Kombinationspräparat;
relativ
langsamer Wirkungseintritt,
Einnahme nach dem Essen |
| |
Mefloquin |
25
mg/kg
(Tag 1: 15 mg/kg;
Tag 2: 10 mg/kg) |
Lariam |
Tag
1 - 2 |
Neurologisch/psychiatrische
Nebenwirkungen
Nicht gleichzeitig Chinin |
| |
Artemether
+ Lumefantrin |
20
mg + 120 mg
je 4 Tabl. 2 x tgl, am ersten Tag in
8 h Abstand |
Riamet |
Tag
1 - 3 |
Nicht
gleichzeitig Chinin |
| Malaria
tropica, kompliziert |
| |
Chinindihydrochlorid
in 5% Glucose |
20
mg/kg als loading dose;
anschließend 10 mg/kg alle 8 h |
|
Tag
1 - 3/7 |
Langsam
über 4 h infundieren;
EKG-Monitoring, Glukose-Monitierung; Vorsicht Umrechnung |
| |
Clindamycin |
2
x tgl 5 - 10mg/kg |
Dalacin
C |
Tag
1 - 5/7 |
Salz-Base |
| |
Artesunat |
2
x 2 mg/kg tgl |
|
Tag
1 - 3 |
Medikament
in Österreich nicht zugelassen |
| |
Mefloquine |
Tag
1: 15 mg/kg;
Tag 2: 10 mg/kg |
Lariam |
Tag
1 - 2 |
Neurolog.
Nebenwirkungen
Nicht gleichzeitig Chinin |
| Malaria
tertiana |
| |
Chloroquin |
Tag
1 + 2: 10 mg/kg Base;
Tag 3: 5 mg/kg Base |
Resochin |
Tag
1 - 3 |
1
Tbl Resochin = 250 mg
Salz = 155 mg Base |
| Plus |
Primaquin |
Tag
4 - 18: 0,25 mg/kg |
|
Tag
4 - 18 |
Ind:
Hypnozoiten-Eradikation
Nur bei normalem G6PD-Status |
| Malaria
tertiana - Chloroquin-Resistenz |
| |
Atovaquone-Proguanil |
15
mg/kg + 6 mg/kg
(1 x tgl 4 Tabletten) |
Malarone |
Tag
1 - 3 |
Kombinationspräparat;
relativ
langsamer Wirkungseintritt,
Einnahme nach dem Essen |
| Oder |
Mefloquine |
Tag
1: 15 mg/kg;
Tag 2: 10 mg/kg |
Lariam |
Tag
1 - 2 |
Neurolog.
Nebenwirkungen
Nicht gleichzeitig Chinin |
| Plus |
Primaquin |
Tag
4 - 18: 0,25 mg/kg |
|
Tag
4 - 18 |
Ind:
Hypnozoiten-Eradikation
Nur bei normalem G6PD-Status |
| Malaria
quartana |
| |
Chloroquin |
Tag
1 + 2: 10 mg/kg Base;
Tag 3: 5 mg/kg Base |
Resochin |
Tag
1 - 3 |
1
Tbl. Resochin = 250 mg
Salz = 155 mg Base |
|
|
| Malaria
und Reisen In
Österreich werden jährlich etwa 100 neue Malariafälle
diagnostiziert. Nahezu 3/4 aller nach Österreich importierten
Malaria-Infektionen werden durch P. falciparum verursacht,
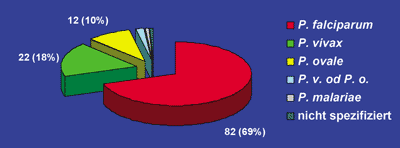
wie aus Abbildung 1 ersichtlich ist. Daten
von 120 Malaria-Patienten aus dem AKH Wien wurden hiefür
zusammengefasst. Weitaus der größte Anteil
dieser Patienten (ca. 80%) hat keinerlei prophylaktische Maßnahmen
getroffen bzw. die Prophylaxen schon während des Aufenthaltes
in der endemischen Region aus verschiedensten Gründen beendet.
Das
Interesse an Tropenkrankheiten im Allgemeinen und an der Malaria
im Speziellen erwacht beim Österreicher im Wesentlichen,
wenn es sich um
eigene Reisen in ferne Länder handelt. Ebenso, wie die
Therapie von Tropenkrankheiten an infektiologischen Zentren
stattfinden sollte, so ist die Beratung der Reisenden durch
die zunehmende Komplexität der epidemiologischen Veränderungen
und den Fortschritt der medizinischen Interventionen nur von
Reisemedizinern nach dem neuesten Stand zu gewährleisten.
Abbildung 1: Verteilung der
Plasmodien-Spezies bei 120 Tropenrückkehrern mit
Malaria im AKH Wien
|
Prinzipiell
ist die Expositionsprophylaxe von besonderer Bedeutung, durch
die das Risiko eines infektiösen Stichs bereits um bis
zu 90% minimiert werden kann. Es handelt sich dabei um Verhaltensmaßnahmen
wie das Vermeiden, sich während der Morgen- und Abenddämmerung
im Freien aufzuhalten, das Tragen von langer heller Bekleidung,
das Benützen von Repellentien, das Schlafen unter Moskitonetzen
und das Imprägnieren von Kleidung und Netzen durch Pyrethroide.
Während diese Maßnahmen äußerst effektiv
sind, haben andere Hilfsmittel wie zum Beispiel die „Ultraschall-Abwehr“
von Moskitos oder die Einnahme von homöopathischen Mitteln
keinen Wert.
Je
nach epidemiologischer Situation sowie Reiseroute und Reisestil
kann eine
Chemoprophylaxe empfehlenswert sein. Trotz zunehmender Resistenzraten
gibt es eine Reihe höchstwirksamer Substanzen (Tabelle
3). Entscheidend scheint auch hier eine ausgewogene und
auf den einzelnen zugeschnittene Beratung zu sein, da jede dieser
Substanzen besondere Nebenwirkungen aufweist und daher nicht
für jeden Reisenden in gleicher Weise in Frage kommt. Wichtig
sei hierbei anzumerken, dass schon vor Reiseantritt mit der
Prophylaxe zu beginnen ist, um einerseits die nötige Plasma-Konzentration
zu gewährleisten und andererseits, um auch eventuell auftretende
Nebenwirkungen frühzeitig erkennen zu können und so
im Bedarfsfall auf ein anderes Medikament umzusteigen. Ein guter
Teil der an Malaria erkrankten Touristen hat
aufgrund von Nebenwirkungen die Einnahme der Malariaprophylaxe
während der Reise ausgesetzt.
Auch
wenn sowohl in der wissenschaftlichen Literatur als auch in
populär-medizinischen Medien immer wieder von Malaria-Vakzinen
gesprochen wird, scheint auch heute, trotz viel versprechender
Ansätze, die Entwicklung eines effektiven Impfstoffs in
weiter Ferne. Kritisch ist auch die Mitgabe von so genannten
Stand-by- oder Notfall-Medikamenten zu diskutieren. Dabei nimmt
der Reisende eine kurative Dosis an Malariamedikamenten mit
und behandelt sich bei fieberhafter Symptomatik selbst. Da dies
zumeist für Gegenden mit niedrigem Malariainfektionsrisiko
empfohlen wird, ist in diesen Fällen durch die vermeintliche
Therapie oft eine Verschleppung der eigentlichen Diagnose zu
befürchten. Leider hat sich auch herausgestellt, dass immun-chromatographische
Kartentests im Ernstfall von betroffenen Touristen zu einem
hohen Prozentsatz nicht ordnungsgemäß durchgeführt
werden und daher nur einen geringen Wert zur Eigendiagnose haben.
Daher scheint es besonders wichtig, alle Reisende aufzuklären,
dass eine schnelle Diagnose durch eine Infektionsabteilung entscheidend
für die weitere Prognose ist.
Tabelle 3: Chemoprophylaxe
der Malaria
| Substanz |
Handelsname |
Dosis |
Tabl |
Einnahmedauer |
Kommentar |
| Chloroquin |
Resochin |
<
75 kg: 300 mg Base/Woche
> 75 kg: 450 mg Base/Woche |
2
Tbl/Woche
3 Tbl/Woche |
1
Woche vor bis
4 Wochen nach |
Aufgrund
hoher Resistenz
nur eingeschränkter Wert |
| Atovaquone/Proguanil |
Malarone |
>
40 kg: 250/100 mg/Tag |
1
Tbl täglich |
1
- 2 Tage vor bis
1 Woche nach |
Einnahme
nach dem Essen |
| Mefloquin |
Lariam |
250
mg/ Woche |
1
Tbl/Woche |
2
Wochen vor bis
4 Wochen nach |
Neuro-psychiatrische
Nebenwirkungen |
| Doxycyclin |
Vibramycin |
100
mg/Tag |
1
Tbl täglich |
2
Tage vor bis
4 Wochen nach |
Kontraindiziert
bei
Kindern und Schwangeren;
Phototoxizität |
| Primaquin |
|
30
mg/kg |
1
x 2 Tbl täglich |
2
Tage vor bis
1 Woche nach |
Nur
bei normalem
G6PD-Status |
Tabelle
4: Malaria-Märchen
| Märchen |
Richtigstellung |
Malaria
ist nie ausheilbar. |
Bei
adäquater Behandlung sowie Eradikationstherapie
der Hypnozoiten (Primaquin) im Falle einer Malaria
tertiana ist jede Malaria ausheilbar. |
Bei
akuter Erkrankung sind die Malariaerreger nur im
Fieberanstieg, nicht aber im fieberfreien Intervall
nachweisbar. |
Parasiten
sind auch zwischen den Fieberepisoden im Dicken
Tropfen nachweisbar, unabhängig vom Fieber
mag zum Teil aufgrund niedriger Parasitämie
eine Wiederholung des Dicken Tropfens nötig
sein. |
Eine
Malariaerkrankung kann auch bei negativem Plasmodiennachweis
vorliegen („Blutausstrich negative Malaria“). |
Eine
akute Erkrankung kann mit negativem Dicken Tropfen
ausgeschlossen werden. Zum Teil kann aufgrund niedriger
Parasitämie eine Wiederholung des Dicken Tropfens
nötig sein. |
Ein
Patient, der nicht fiebert, kann nicht an Malaria
erkrankt sein. |
Zumeist
berichtet der Patient über Fieber, wenn er
auch zum Untersuchungszeitpunkt fieberfrei ist.
Dennoch ist eine Malaria auch ohne das Auftreten
von Fieber nicht auszuschließen. |
Der
Patient wurde von Ärzten im Endemiegebiet nach
den dortigen Empfehlungen behandelt. |
Bei
Bewohnern endemischer Gebiete können aufgrund
der Semi-Immunität Medikamente wirksam sein,
die bei Personen aus Nichtendemiegebieten („Tropenreisende“)
nicht mehr kurativ sind. |
Die
Mefloquintherapie muss bis zum Sistieren des Fiebers
fortgeführt werden. |
Mefloquin
sollte nur für 2 Tage verabreicht werden. Bei
Therapieversagern (selten!) ist eine Umstellung
auf andere Medikamente durchzuführen. Bei Überdosierung
können schwere neurologisch/psychiatrische
Nebenwirkungen auftreten. |
|
|
| Zusammenfassung
Auch
zu Beginn des 21. Jahrhunderts hat die Malaria nichts an ihrer
Bedeutung verloren. Trotz viel versprechender Erkenntnisse und
Fortschritte in der tropenmedizinischen Forschung ist es in
den letzten Jahrzehnten zu einer weiteren geographischen Ausbreitung
und Zunahme der Malariamorbidität und -mortalität
gekommen. Trotz der viel diskutierten Erderwärmung ist
aufgrund der gut funktionierenden Gesundheitssysteme nicht mit
einer Rückkehr der endemischen Malaria in Europa zurechnen.
Dennoch wird es durch die Zunahme an Fernreisen im Zeitalter
der globalisierten Welt zweifellos zu einem
Anstieg an importierten Malariafällen in Österreich
kommen.
Für Reisende und Reiserückkehrer ist die gewissenhafte
Beratung durch spezialisierte Institutionen unerlässlich.
Für Patienten sind das schnelle Reagieren und die unverzügliche
Diagnosestellung von mitunter lebensrettender Bedeutung. Dies
bedeutet für Ärzte vor allem eines: Bei beinahe allen
Symptomen nach Tropenaufenthalt an Malaria zu denken und die
entsprechende Diagnosestellung einzuleiten. Die wahre Bürde
der Malaria – sowohl in menschlicher, medizinischer als
auch in ökonomischer Sicht – hat allerdings auch
heute noch die Bevölkerung der tropischen Länder zu
tragen.
|
|
|