Pharmakokinetische
Aspekte zur Findung des geeigneten Antibiotikums |
| C. Joukhadar
Univ.-Klinik für Klinische Pharmakologie, Abteilung für
Klinische Pharmakokinetik, Medizinische Universität Wien
(Vorstand: Univ.-Prof. Dr. Markus Müller) |
|
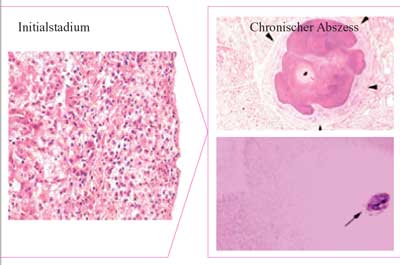
| Abszesse
bestehen aus einer äußeren Membran bzw. Kapsel, einer
inneren Leukozytenschicht und zentralen nekrotischen Zellbestandteilen
(Abbildung 1). Lokalisation und Morphologie
sind variabel, ebenso können die Erreger zu verschiedenen
bakteriellen Spezies gehören.
Eine antibiotische Therapie von Abszessen gestaltet sich oft
schwierig, nach Möglichkeit sollte chirurgisch drainiert
werden. Die Wirksamkeit antiinfektiver Substanzen wird durch
schlechte Permeabilität, geringe Sauerstoffverfügbarkeit
und niedrigen pH eingeschränkt. Ein Problem ist auch das
verlangsamte Bakterienwachstum in der eitrigen Abszessflüssigkeit,
da Antibiotika meist gerade in der Wachstumsphase angreifen.
Abbildung
1: Abszessmorphologie: äußere Membran/Kapsel,
innere Leukozytenschicht und zentrale nekrotische Zellbestandteile
|
Das ideale Antibiotikum
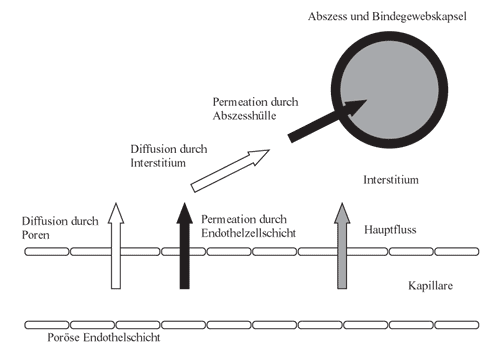
Bis das
Antibiotikum im Abszessinneren wirken kann, hat es einen pharmakokinetischen
Hürdenlauf zu bewältigen (Abbildung
2). Zunächst muss die Substanz aus dem Gefäßsystem
über kapillare Poren durch das Endothel ins Interstitium
gelangen, zum Abszess diffundieren und anschließend
durch die Kapsel in das Innere des Abszesses penetrieren.
Bei der Auswahl des idealen Antibiotikums müssen daher
eine ausreichende Abszess-Penetration, geringe Proteinbindung,
antibakterielle Aktivität im anaeroben Milieu und ein
genügend breites antibiotisches Spektrum gefordert werden.
Die Anforderungen sind nicht einfach zu erfüllen. Das
ideale Antibiotikum sollte eine vernachlässigbare Proteinbindung
und ein hohes Verteilungsvolumen besitzen – zwei Forderungen,
die letztendlich im Gegensatz zueinander stehen und von einem
einzelnen antimikrobiellen Wirkstoff auch nicht erfüllbar
sind. Darüber hinaus wäre eine Potenzierung der
antibiotischen Aktivität im anaeroben Milieu wünschenswert.
Dass das Wirkspektrum des Antibiotikums natürlich auch
alle zu erwartenden Erreger inkludieren sollte, versteht sich
von selbst.
Abbildung
2: Der pharmakokinetische Hürdenlauf eines Antibiotikums
|
Studie mit Fosfomycin
Die
Messung des zeitlichen Konzentrationsverlaufes eines Antibiotikums
im Abszess ist eine Herausforderung, da aus einem Abszess nur
einmal eine Probe gewonnen werden kann. Daher wurde in einer
Studie an 18 Patienten (Alter 18-80 Jahre) nach intravenöser
Gabe von 8 Gramm Fosfomycin die Abszessgröße bestimmt,
regelmäßig Blut abgenommen und Abszessflüssigkeit
zu unterschiedlichen Zeitpunkten im Rahmen einer interventionellen
Abszessdrainage gewonnen. Die Ergebnisse wurden entsprechend
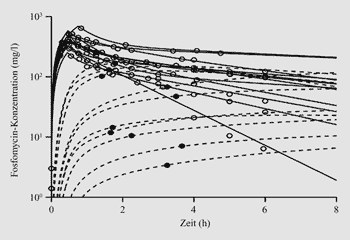
extrapoliert (Abbildung 3). Es konnte keine
Korrelation zwischen der Plasma- und der Abszess-Pharmakokinetik,
jedoch eine sehr gute Korrelation der Permeabilitätsfähigkeit
und der Abszess-Pharmakokinetik gefunden werden. Die Halbwertszeit
von Fosfomycin im Abszess war in den meisten Fällen deutlich
verlängert. Laut der Studie sollten hohe Dosen verabreicht
und eine Ladungsdosis nicht vergessen werden, um rasch hohe
Konzentrationen im Abszess zu erreichen. Bei Niereninsuffizienz
ist die Dosierung zu reduzieren, die Ladungsdosis bleibt aber
unverändert. Trotz der sehr hohen interindividuellen Variabilität
konnten im Steady State bei fast allen Patienten effektive Fosfomycin-Konzentrationen
im Abszess erreicht werden. Daher ist die Gabe von Antibiotika
wie Fosfomycin eine sinnvolle therapeutische Option, wenn eine
chirurgische Sanierung nicht durchführbar ist.
Abbildung
3: Verläufe der gemessenen Plasmakonzentrationen
(°) und extrapolierten Abszesskonzentrationen (•)
(Sauermann, Joukhadar et al., AAC 2005)
|
Anschrift
des Referenten:
Univ.-Prof. Dr. Christian Joukhadar
Univ.-Klinik für Klin. Pharmakologie, Abt. für Klin. Pharmakokinetik
A-1090 Wien, Währinger Gürtel 18-20
E-Mail: christian.joukhadar@meduniwien.ac.at
|