H. Burgmann
Univ.-Klinik für Innere Medizin I, Klin. Abt. für
Infektionen und Tropenmedizin, Medizinische Universität
Wien |
|
|
|
Piperacillin/Tazobactam
Piperacillin/Tazobactam ist ein Breitspektrum-Antibiotikum
mit ausgezeichnetem Wirk- und Sicherheitsprofil. Es findet Verwendung
in der Therapie zahlreicher Infektionen [1].
Aufbau
Piperacillin (Abbildung 1) (Molekulargewicht: 539,5) ist ein
semisynthetisches Ureidopenicillin mit antibakterieller Aktivität
gegen Gram-positive und Gram-negative Aerobier- und Anaerobierbakterien.
Die Verwendung von Piperacillin wurde allerdings durch das vermehrte
Auftreten von Betalaktamase-produzierenden Bakterien eingeschränkt.
Tazobactam (Abbildung 2) [2] (Molekulargewicht:
322,3) ist ein synthetisches Penicillansäuresulfon, welches
einen Betalaktam-Ring besitzt und sich von der 6-Aminopenicillansäure
ableitet. Es wirkt als Betalaktamasehemmer und schützt Piperacillin
vor der Zerstörung durch Betalaktamaseenzyme. Wenn es mit
Piperacillin kombiniert wird, wird das Spektrum auf zahlreiche
Betalaktamaseproduzierte Keime inklusive Staphylokokken und viele
Enterobakterien, Haemophilus influenzae und Bacteroides
spp. erweitert. |
| Pharmakodynamik
Wie
andere Betalaktame entfaltet Piperacillin seine bakterizide
Aktivität durch Bindung an das Penicillin-bindende Protein
der Bakterienzellwand. Dies führt zu einer Hemmung der
Zellwandsynthese und evtl. zur Zelllyse.
Tazobactam hemmt irreversibel viele Betalaktamasen, die von
wichtigen Gram-negativen oder Gram-positiven aeroben oder anaeroben
Bakterien produziert werden. Tazobactam hat eine sehr niedrige
Affinität für Penicillinbindende Proteine und zeigt
daher eine sehr geringe intrinsische antibakterielle Aktivität.
Wirksamkeit
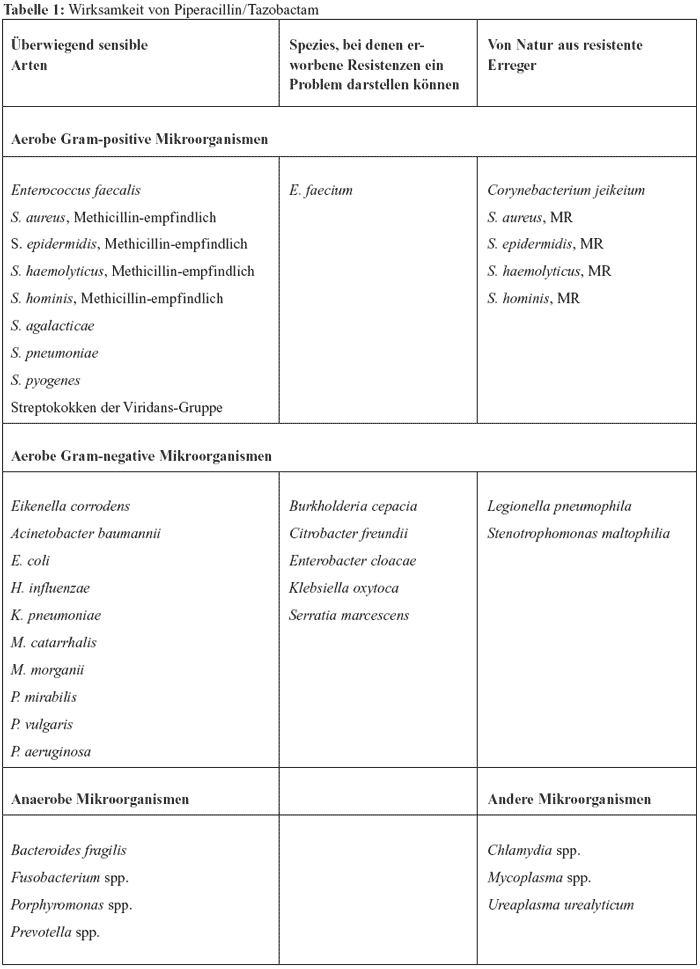
Gram-positive Bakterien
Piperacillin/Tazobactam zeigt eine gute In vitro-Aktivität
gegenüber dem Großteil von Gram-positiven Bakterien
inklusive der Betalaktamase-produzierenden.
Piperacillin/Tazobactam entfaltet gute Wirksamkeit gegen Methicillin-/Oxacillin-empfindliche
Stämme von Staphylococcus aureus und Koagulase-negativen
Staphylokokken. Wie andere Betalaktam/Betalaktamasekombinationen
ist Piperacillin/Tazobactam unwirksam gegenüber Methicillin-
resistenten S. aureus und ist generell inaktiv gegenüber
anderen Stämmen von Methicillin-resistenten Staphylokokken
inkl. Methicillin-resistenter Koagulasenegativer Staphylokokken.
Penicillin-empfindliche
Streptococcus pneumoniae-Stämme sind hoch empfindlich
gegenüber Piperacillin/Tazobactam. Pip/Taz zeigt aber auch
gute Aktivität gegen intermediär und Penicillin-resistente
Pneumokokken.
Piperacillin/Tazobactam zeigt auch Aktivität gegenüber
Enterococcus faecalis, während Enterococcus
faecium-Stämme resistent sind.
Gram-negative Bakterien
Piperacillin/Tazobactam ist aktiv gegenüber einem Großteil
von Plasmid-mediierten, Betalaktamase-produzierenden (und nicht
Betalaktamase-produzierenden) Gramnegativen Bakterien. Einige
Non-Fermenter sind ebenfalls empfindlich auf die Kombination.
Enterobakterien: Stämme von E. coli, S. marcescens,
Proteus mirabilis, Proteus vulgaris, Klebsiella
pneumoniae, Klebsiella oxytoca (und anderen Klebsiella
spp.), Enterobacter aerogenes und Citrobacter
spp. sind generell empfindlich oder intramediär empfindlich
auf Piperacillin/Tazobactam. Andererseits gibt es aber auch
Hinweise von Resistenz gegenüber einigen Citrobacter
freundii- und Enterobacter cloacae-Stämmen.
Andere Gram-negative Bakterien
Piperacillin/Tazobactam zeigt exzellente Aktivität gegenüber
Betalaktamase- und nicht Betalaktamase-produzierenden Stämmen
von Haemophilus influenzae und Moraxella catarrhalis.
Non-Fermenter
Piperacillin/Tazobactam ist aktiv gegen Piperacillin-empfindlich
Stämme von Pseudomonas aeruginosa. Auch andere
Stämme von Pseudomonas befinden sich im Wirkspektrum.
Piperacillin/Tazobactam zeigt auch gute Aktivität gegenüber
Acinetobacter spp.
Piperacillin ist instabil gegen Betalaktamasen und wird durch
diese zerstört. Tazobactam inaktiviert zahlreiche klinisch
relevante Betalaktamasen. Besondere Aufmerksamkeit wird unter
anderem den Extended-Spectrum-Betalaktamasen (ESBL) gewidmet,
da diese weltweit zunehmen und die meisten Substanzen der Betalaktamgruppe
betreffen. Tazobactam ist in vitro der effizienteste
Inhibitor auch bei ESBL [3]. Studien haben gezeigt, dass Piperacillin/Tazobactam
auch bei ESBL-produzierenden Keimen effektiv eingesetzt werden
kann.
Anaerobier
Piperacillin/Tazobactam ist höchst aktiv gegen Bacteroides
fragilis (inklusive Cefoxitin- und Clindamycin-resistenter
Stämme). Die Aktivität ist zumindest genauso gut wie
die von Ampicillin/Sulbactam oder Amoxicillin/Clavulansäure.
Andere Anaerobier wie Clostridium spp., Fusobacterium
spp., Peptostreptococcus spp. und Peptococcus
spp. werden ebenfalls gut durch Piperacillin/Tazobactam abgedeckt.
|
| Pharmakokinetik
[4, 5] Weder
Piperacillin noch Tazobactam werden aus dem Gastrointestinaltrakt
resorbiert. Die Kombination Piperacillin/Tazobactam wird als
langsamer Bolus oder als Infusion in einer 8:1- oder 4:1-Ratio
verabreicht. Die beiden Substanzen können gleichzeitig
verabreicht werden, da sie ähnliche pharmakokinetische
Profile bei Erwachsenen und Kindern aufweisen. Zunehmend an
Bedeutung erreichte in den letzten Jahren die prolongierte bzw.
auch kontinuierliche Verabreichung von Piperacillin/Tazobactam
[6, 7, 8]. So konnten Lorente et al. bei Patienten mit Gram-negativer
Respirationspneumonie höhere klinische Heilungsraten bei
kontinuierlicher Gabe beobachten. Lodise et al. [9] zeigten
bei kritisch kranken Patienten mit P. aeruginosa-Infektion
signifikant geringere 14-Tage-Mortalität bei prolongierter
Verabreichung von Piperacillin/Tazobactam in Vergleich zu Bolusapplikation
(30 min) (12,2 vs. 31,6%).
Die Spitzenkonzentrationen im Serum werden unmittelbar nach
intravenöser Gabe erreicht.
Die
mittlere maximale Plasmakonzentration (Cmax) von Piperacillin/Tazobactam
schwankte nach einer Einmalgabe von 4/0,5 g Piperacillin/Tazobactam
bei gesunden erwachsenen Probanden zwischen 264,4 bis 368 und
29,1 - 39 mg/l. Es konnte weder bei Piperacillin noch bei Tazobactam
ein Hinweis auf Akkumulation nach der Verabreichung von multiplen
Dosen bei gesunden Probanden oder bei Patienten mit Infektionen
beobachtet werden. Nach mehrfacher Gabe (4/0,5 g 6- oder 8-stündlich)
war die Ratio von Piperacillin Cmax zu Tazobactam Cmax ungefähr
8 zu 1.
Verteilung
Das Verteilungsvolumen von Piperacillin im Steady-State reicht
von 15 - 21 Litern (bei Gesunden oder bei Patienten mit Infektionen).
Die korrespondierenden Werte von Tazobactam waren 18 - 34,6
Liter. Piperacillin und Tazobactam werden beide zu ungefähr
20% an Plasmaprotein gebunden. Die Verteilung von Piperacillin
und Tazobactam erfolgt rasch innerhalb von 30 Minuten nach dem
Ende einer 30-minütigen Infusion. Beide Komponenten sind
hydrophil und penetrieren gut in unterschiedliche Gewebe und
Körperflüssigkeiten.
Metabolismus und Elimination
Bei den Erwachsenen werden ungefähr 50 - 60% der verabreichten
Dosis von Piperacillin und Tazobactam renal durch glomeruläre
Filtration und tubuläre Sekretion ausgeschieden. Bei einmaliger
oder mehrmaliger Verabreichung von Piperacillin und Tazobactam
an gesunden Probanden lag die Plasmahalbwertszeit von Piperacillin
und Tazobactam zwischen 0,7 und 1,2 Stunden und war von der
Dosis und der Infusionszeit unabhängig.
Tazobactam führt zu keiner signifikanten Veränderung
der Pharmakokinetik von Piperacillin. Piperacillin scheint die
Eliminationsrate von Tazobactam zu verringern.
Die biliäre Exkretion beträgt etwa 2% der verabreichten
Dosis. Die mittlere Konzentration von Piperacillin in der Gallenblase
war mehr als 10-fach höher als die Plasma-Piperacillin-Konzentration,
was wiederum auf einen aktiven Sekretionsprozess in die Galle
hinweisen würde. So ein aktiver Transport konnte für
Tazobactam nicht beobachtet werden.
Piperacillin und Tazobactam haben beide eine mittlere Plasmaeliminationshalbwertszeit
von ungefähr 0,8 - 1 Stunde.
Metabolismus: Piperacillin wird zu einem unbedeutenden mikrobiologisch
aktiven Desethyl-Metaboliten abgebaut. Tazobactam wird zu einem
einzigen Metaboliten abgebaut, der mikrobiologisch inaktiv ist.

|
Pharmakokinetik
bei speziellen Patientenpopulationen Patienten
mit renalen Störungen
Ähnlich wie bei anderen Betalaktamaseinhibitorkombinationen
steigt die Plasmakonzentration von Piperacillin und Tazobactam
beträchtlich an und die Halbwertszeit verlängert sich
bei Patienten mit renaler Insuffizienz. Bei einer Kreatininclearance
< 20 ml/min verdoppelt sich die Halbwertszeit von Piperacillin,
die von Tazobactam vervierfacht sich. Daher wird bei einer Kreatininclearance
unter 20 ml pro Minute eine Dosisreduktion empfohlen.
Hämodialyse entfernt etwa 30 - 40% von Piperacillin/Tazobactam.
Peritonealdialyse entfernt 6% von Piperacillin und 21% der Tazobactamdosis.
Patienten
mit hepatischen Störungen
Die Pharmakokinetik von Piperacillin und Tazobactam wird bei
Patienten mit hepatischen Störungen nicht signifikant verändert.
Septischer
Patient
Zahlreiche Studien belegen eine Veränderung der Pharmakokinetik
bei Patienten mit schwerem Schock [10]. Einerseits kann durch
Ödeme, Pleuraergüsse oder Aszites eine Erhöhung
des Verteilungsvolumens beobachtet werden, andererseits nimmt
die Clearance durch den hyperdynamischen Kreislauf zu. Für
Piperacillin konnten 5-10-fach geringere Gewebespiegel mittels
Mikrodialyse im Vergleich zu den korrespondierenden Plasmawerten
gemessen werden [11]. Bei diesen Patienten wird daher eine Dosis-erhöhung
auf 4 x 4,5 g/Tag empfohlen.
Kleinkinder und Kinder
Keine dosisabhängigen Differenzen der Pharmakokinetik von
Piperacillin und Tazobactam betreffend Cmax und AUC wurden bei
Kindern und Kleinkindern mit Infektionen gefunden. Bei Säuglingen
unter 6 Monaten war allerdings die Halbwertszeit länger
und die totale Körperclearance geringer als bei Kindern
über 6 Monaten. Daher sollte bei diesen Patienten die Dosis
modifiziert werden. |
| Anwendungsgebiete
Piperacillin/Tazobactam
ist zur Behandlung folgender systemischer und/oder lokaler bakterieller
Infektionen angezeigt, bei denen empfindliche Erreger nachgewiesen
und vermutet werden können.
- Außerhalb
des Krankenhauses erworbene Pneumonie (ausschließlich
mäßiger Schweregrad),
- nosokomiale
Pneumonie (mäßig bis schwer),
-
außerhalb des Krankenhauses erworbene Haut- und Weichteilinfektionen,
- komplizierte
Harnwegsinfektionen,
- intraabdominelle
Infektionen,
-
bakterielle Infektionen bei neutropenischen Erwachsenen.
|
| Dosierung
Die
Gesamtdosis hängt von der Schwere und Lokalisation der
Infektion, der Empfindlichkeit des Erregers und dem Krankheitszustand
des Patienten ab und kann bis zu 3 – 4 x 4,5 g (4 g Piperacillin/500
mg Tazobactam) betragen. Höhere Dosierungen von 4 g Piperacillin/0,5
g Tazobactam alle 6 Stunden werden zur Behandlung von Patienten
mit schwerer Infektion einschließlich febriler Neutropenie
verwendet. Die empfohlene Tagesdosis liegt üblicherweise
zwischen 100 und 200 mg Piperacillin pro kg Körpergewicht.
Bei Patienten mit Niereninsuffizienz sollte die intravenöse
Dosis der Einschränkung der Nierenfunktion angepasst werden.
Bis zu einer Kreatininclearance von 20 ml/min kann ein normales
Dosierungsintervall (8 Stunden) beibehalten werden. Wenn die
Kreatininclearance weniger als 20 ml/min ist oder der Patient
dialysiert wird, sollte das Dosierungsintervall auf 12 Stunden
verlängert werden. Bei Patienten mit Hämodialyse beträgt
die maximale Dosis 4 g Piperacillin und 0,5 g Tazobactam 2 x
täglich. Da durch die Hämodialyse 30 - 50% des Piperacillins
und ca. 39% des Tazobactams in 4 Stunden entfernt werden, soll
eine zusätzliche Dosis von 2 g Piperacillin und 0,25 mg
Tazobactam nach jeder Dialyseperiode verabreicht werden. Durch
Peritonealdialyse (CAPD) werden nur 5% der Piperacillin- und
12% der Tazobactam-Dosis entfernt. Eine zusätzliche Dosis
wie bei der Hämodialyse ist nicht erforderlich (Tabelle
3).
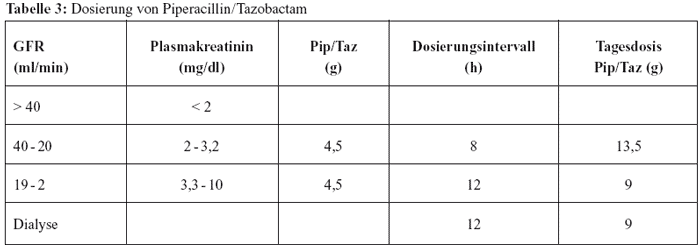
Bei Patienten mit Hämodialyse beträgt die Maximaldosis
8 g Piperacillin und 1 g Tazobactam.
Dosierung bei Kindern
Für 2 - 12-jährige Kinder mit Körpergewicht bis
zu 40 kg und normaler Nierenfunktion beträgt die empfohlene
Dosis 112,5 mg/kg KG (100 mg Piperacillin/12,5 mg Tazobactam)
alle 8 Stunden. Bei Kindern über 40 kg Kg wird die Erwachsenendosis
angewendet.
Piperacillin/Tazobactam wird weitgehend in den Geweben und Körperflüssigkeiten
einschließlich der Darmschleimhaut, Gallenblase, Lunge,
Galle und Knochen verteilt. Die mittleren Gewebekonzentrationen
belaufen sich in der Regel auf 50 - 100% der Konzentrationen
in Plasma. Konzentrationen von Piperacillin/Tazobactam in unterschiedlichen
Geweben/Flüssigkeiten nach single dose (SD) oder Mehrfachapplikation
als iv -Infusion über 30 min (Tabelle 4).
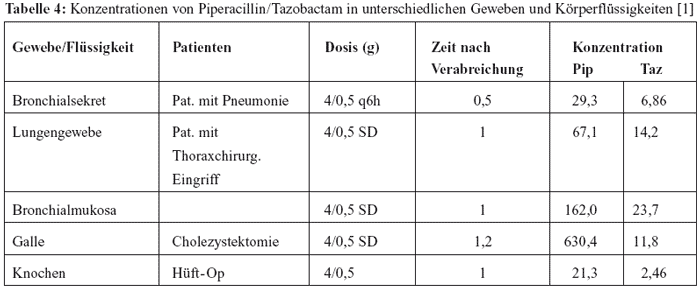
Neuere Studien belegen auch eine exzellente Gewebeanreicherung
im Pankreassaft [12] bzw. Kiefer- und Hüftknochen [13].
Nebenwirkungen
Am häufigsten treten gastrointestinale Störungen auf,
selten zentralnervöse, kardiovaskuläre Beeinträchtigungen
sowie pseudomembranöse Enterokolitis. Weiters werden selten
vorübergehender Anstieg der Leberenzyme und des Bilirubins
im Blut sowie cholestatische Hepatitis beobachtet (Tabelle 5).

|
| Klinische
Beurteilung Die
fixe Kombination von Piperacillin/Tazobactam stellt ein bewährtes
Therapiekonzept bei der Therapie schwerer Infektionen dar. Das
breite Wirkspektrum umfasst fast alle relevanten Gram-positiven
und Gram-negativen Erreger.
Als Indikation für Piperacillin/Tazobactam ergeben sich
Infektionen, bei denen unter anderem Pseudomonas aeruginosa
eine potenzielle Rolle haben könnte, z. B. der neutropenische
bzw. der Verbrennungspatient, Patienten mit intraabdominellen
Atemwegs- und Weichteilinfektionen [14] (siehe Tabelle 6).
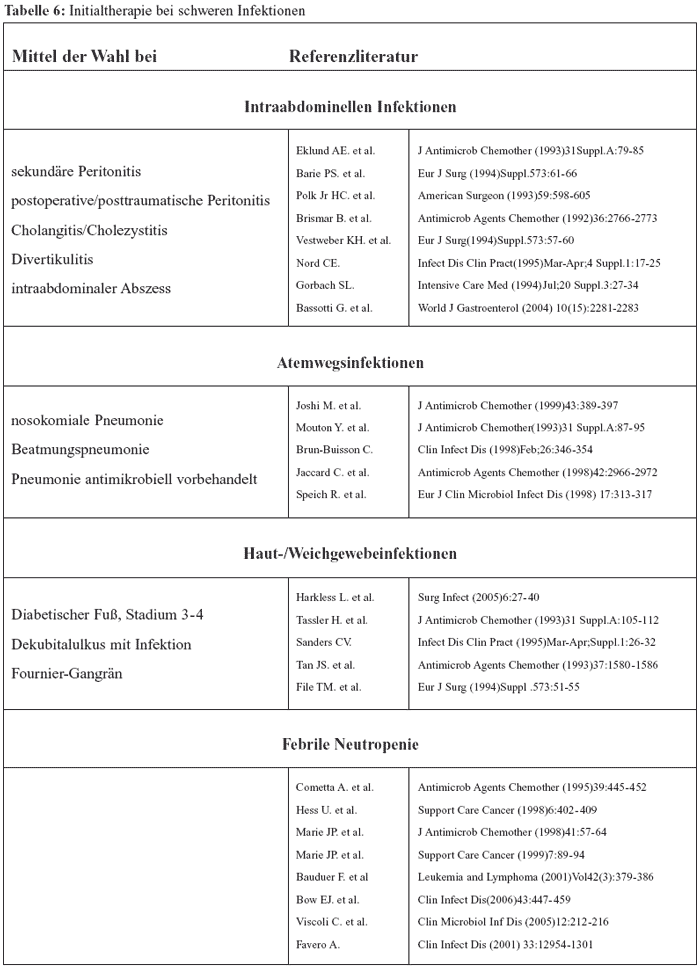
Die Dosierung ist mit 3 x 4,5 bis 4 x 4,5 schon deutlich höher
als die der anderen Betalaktamase-Kombinationen, was in der
hohen MHK von Pseudomonas aeruginosa begründet
liegt. Wesentlicher Teil der positiven Einschätzung ist
die hohe Dosierungsmöglichkeit, bedingt durch eine große
therapeutische Breite.
Die aktuelle klinische Literatur zur Anwendung von Piperacillin/Tazobactam
belegt auch heute noch eine gute Wirksamkeit. Beispielsweise
konnte in einer Studie zu Bauchrauminfektionen eine klinische
Heilung bei 97% der Patienten erreicht werden.
Bodmann et al [15] berichten über eine insgesamt 87,5%
die klinische Effektivität bei einer Vielzahl im Routinebetrieb
behandelnder Infektionen aus dem Zeitraum 2000 - 2004. In dieser
Studie wurde die Wirksamkeit und Sicherheit der Anwendung der
fixen Kombination von Piperacillin/ Tazobactam in der Behandlung
ein breites Spektrum mittlerer bis schwerer nosokomialer sowie
außerhalb des Krankenhauses erworbener Infektionen in
der klinischen Praxis untersucht. Es wurden 9488 hospitalisierte
Patienten mit unterschiedlichen Infektionen, vorwiegend im Bereich
der Atemwege, der Haut- und des Weichgewebes, sowie intraabdominellen
Infektionen untersucht. Es wurden ausführliche Daten zur
antibiotischen Therapie sowie zur klinischen und mikrobiologischen
Wirksamkeit sowie zum Profil der beobachtenden unerwünschten
Arzneimittelwirkungen gesammelt. Bei der Anwendung von Piperacillin/Tazobactam
in der Standarddosierung konnten in Abhängigkeit von der
Schwere der Lokalisation der Infektionen sehr gute klinische
Ansprechraten von bis zu 93,7% beobachtet werden. Lediglich
bei 1,5% der Patienten wurden unerwünschte Arzneimittelwirkungen,
am häufigsten Diarrhoe, beobachtet.
Auch für die empirische Behandlung des neutropenischen
Patienten stellt Piperacillin/Tazobactam eine bewährte
Therapiestrategie dar [16] (Tabelle 7).

|
| Zusammenfassung
Die
fixe Kombination von Piperacillin/Tazobactam stellt auch heute
noch ein effektives Therapiekonzept bei der Therapie schwerer
Infektionen dar. Aufgrund der großen therapeutischen Breite
kann Piperacillin/Tazobactam hoch dosiert werden, ein Umstand,
der besonders bei Intensiv- oder neutropenischen Patienten eine
bedeutende Rolle spielt. Die Wirksamkeit bei einerseits P.
aeruginosa als auch bei Penicillinase-bildenden Staphylokokken
ermöglicht den empirischen Einsatz der Kombination bei
nosokomialen Infektionen und bei granulozytopenischen Patienten.
Durch die Wirkung im anaeroben Bereich empfiehlt sich Piperacillin/Tazobactam
für den Einsatz bei abdominellen Infektionen. |
Literatur
| 1.
Perry CM, Markham A. Piperacillin/tazobactam: an updated
review of its use in the treatment of bacterial infections.
Drugs 1999; 57: 805-43. |
| 2.
Pena Amparo de la GA, Derendorf Hartmut. Pharmakokinetik
von Betalaktamase-Inhibitoren bei eingeschränkter Nierenfunktion.
Chemotherapie Journal 2000. |
| 3.
Peterson LR. Antibiotic policy and prescribing strategies
for therapy of extended-spectrum beta-lactamase-producing
Enterobacteriaceae: the role of piperacillin-tazobactam.
Clin Microbiol Infect 2008; 14 Suppl 1: 181-4. |
| 4.
Sorgel F, Kinzig M. Pharmacokinetic characteristics of piperacillin/tazobactam.
Intensive care medicine 1994; 20 Suppl 3: 14-20. |
| 5.
Sorgel F, Kinzig M. The chemistry, pharmacokinetics and
tissue distribution of piperacillin/tazobactam. The Journal
of antimicrobial chemotherapy 1993; 31 Suppl A: 39-60. |
| 6.
Boselli E, Breilh D, Rimmele T, et al. Alveolar concentrations
of piperacillin/tazobactam administered in continuous infusion
to patients with ventilator-associated pneumonia. Critical
care medicine 2008; 36: 1500-6. |
| 7.
Buck C, Bertram N, Ackermann T, Sauerbruch T, Derendorf
H, Paar WD. Pharmacokinetics of piperacillin-tazobactam:
intermittent dosing versus continuous infusion. International
journal of antimicrobial agents 2005; 25: 62-7. |
| 8.
Roberts JA, Roberts MS, Robertson TA, Dalley AJ, Lipman
J. Piperacillin penetration into tissue of critically ill
patients with sepsis-bolus versus continuous administration?
Critical care medicine 2009; 37: 926-33. |
| 9.
Lodise TP, Jr., Lomaestro B, Drusano GL. Piperacillin-tazobactam
for Pseudomonas aeruginosa-infection: clinical implications
of an extended-infusion dosing strategy. Clin Infect Dis
2007; 44: 357-63. |
| 10.
Brunner M, Pernerstorfer T, Mayer BX, Eichler HG, Muller
M. Surgery and intensive care procedures affect the target
site distribution of piperacillin. Critical care medicine
2000; 28: 1754- 9. |
| 11.
Joukhadar C, Frossard M, Mayer BX, et al. Impaired target
site penetration of betalactams may account for therapeutic
failure in patients with septic shock. Critical care medicine
2001; 29: 385-91. |
| 12.
Bertazzoni Minelli E, Benini A, Franco L, Bassi C, Pederzoli
P. Piperacillin-tazobactam penetration into human pancreatic
juice. Antimicrobial agents and chemotherapy 2008; 52: 4149-52. |
| 13.
Al-Nawas B, Kinzig-Schippers M, Soergel F, Shah PM. Concentrations
of piperacillin-tazobactam in human jaw and hip bone. J
Craniomaxillofac Surg 2008; 36: 468-72. |
| 14.
Legat FJ, Krause R, Zenahlik P, et al. Penetration of piperacillin
and tazobactam into inflamed soft tissue of patients with
diabetic foot infection. Antimicrobial agents and chemotherapy
2005; 49: 4368-71. |
| 15.
Bodmann KF, Karin Spieker. Klinische Wirksamkeit und Verträglichkeit
von Piperacillin/Tazobactam in der Routineanwendung. Chemotherapie
Journal 2007. |
| 16.
Fanci R, Bartolozzi B, Longo G, Bosi A. A prospective, openlabel
noncomparative study with piperacillin-tazobactam monotherapy
as management of fever in patients with acute leukemia.
Journal of chemotherapy (Florence, Italy) 2008; 20: 492-6. |
Anschrift
des Verfassers:
A.o. Univ.-Prof. Dr. Heinz Burgmann
Univ.-Klinik für Innere Medizin I
Klin. Abt. f. Infektionen und Tropenmedizin
1090 Wien,Währinger Gürtel 18-20
E-Mail: heinz.burgmann@meduniwien.ac.at
|
|
|