|
Natürlicher Verlauf
Über
den natürlichen Verlauf einiger der heute als Manifestation
der Lyme-Borreliose bekannten Erkrankungen des Menschen wissen
wir aus zahlreichen Berichten, die vor der Entdeckung der Krankheitserreger
gemacht worden sind.
Das beginnt mit der Beschreibung einer „diffusen, idiopathischen
Hautatrophie“ durch Alfred Buchwald aus Breslau im Jahr
1883, die bei einem 36-jährigen Patienten bereits über
16 Jahre bestanden hatte. 1902 beschrieben Herxheimer und Hartmann
die Entwicklung dieser Hauterkrankung von einer frühen
entzündlichen Phase in eine späte chronische und benannten
das Krankheitsbild Acrodermatitis chronica atrophicans. Das
gesamte Spektrum der Erscheinungen wurde dann in den Jahren
danach beschrieben, nämlich Haarverlust, makuläre
Atrophie (Anetoderma), sklerodermieartige Veränderungen,
ulnare Bänder, fibroide Knoten und das typische Erscheinungsbild
der chronisch atrophischen Haut, wie „zerknülltes
Zigarettenpapier“. In den 1920er Jahren beschrieben Jessner
und Ehrmann & Falkenstein, dass einige Patienten an Gelenksschmerzen
litten, bevor sich die Acrodermatitis chronica atrophicans entwickelte
und Jessner & Loewenstamm berichteten, dass bei mehr als
10% dieser Patienten Gelenksveränderungen vorlagen. Hanns
Christian Hopf wies in den 1960er Jahren an einem großen
Patientengut nach, dass die periphere Neuropathie vom distalen
Typ ein Teil des klinischen Bildes bei länger bestehender
Acrodermatitis chronica atrophicans ist. Er beschrieb auch Begleiterscheinungen
der Acrodermatitis wie Arthritis und Arthralgien, Herzerkrankungen
und zerebrale Beteiligung.
Weiter wiesen Ehrmann und Falkenstein (1925) auf eine Analogie
der histologischen Veränderungen bei Syphilis und Acrodermatitis
chronica atrophicans hin, die auf der großen Zahl von
Plasmazellen und der Ausbreitung der entzündlichen Infiltrate
entlang der perivenösen Lymphgefäße beruhte.
Sie postulierten die kontinuierliche Ausbreitung des „Virus“
entlang der Gefäße sowie seine gelegentliche Ausbreitung
über die Blutbahn. Wilhelm Balban aus Wien beschrieb 1910
detailliert die Entwicklung von annulären Erythemen bei
drei Patienten. Und 1913 beschrieb Benjamin Lipschütz,
ebenfalls aus Wien, einen Fall von „Erythema chronicum
migrans“. Er beobachtete die Ausbreitung der Hautläsion,
die von der Kniekehle ausging, über sieben Monate. Das
Erythem erstreckte sich schließlich über den Oberschenkel
und den Rücken bis zum Nacken und schwand dann spontan.
In der Abbildung 1 a-f ist die Entwicklung eines über mehr
als 1 Monat „gewachsenen“ Erythema migrans dargestellt.
Zwei Wochen nach einem Zeckenstich hat sich ein roter Fleck
um die Stichstelle gebildet und kontinuierlich ausgedehnt, bis
er nach mehr als einem Monat einen Durchmesser von mehr als
25 cm erreicht hat. Zu dem Zeitpunkt wurde die Behandlung begonnen.
Die Patientin hatte unspezifische Begleiterscheinungen, die
sie aber zuerst nicht mit der Hautrötung in Zusammenhang
sah. Allerdings war sie nach der erfolgreichen Behandlung mit
einem geeigneten Antibiotikum völlig frei von Gelenks-
und Muskelschmerzen sowie Müdigkeit und Erschöpfung.
In
einem anderen Fall war die Hautläsion anfänglich von
Juckreiz um die Zeckenstichstelle begleitet, weshalb die Hautstelle
aufgekratzt wurde. Innerhalb eines Monates entwickelte sich
schließlich ein ringförmiges Erythema migrans (Abbildung
2a, b).
Im
Jahr 1911 beschrieb Jean Louis Burckhardt aus Basel erstmals
ein solitäres Lymphozytom, das bei einer 60-jährigen
Frau als erythematöser Plaque (2 x 6 cm) über einige
Wochen am Oberarm zu beobachten war.
Histologisch
zeigte sich Lymphgewebe mit Keimzentren, einem Lymphknoten vergleichbar.
Biberstein verwendete erstmals 1923 den Begriff Lymphozytom.
Schließlich gab Bo Bäfverstedt aus Stockholm eine
umfassende Darstellung von gutartigen solitären und multiplen
Pseudolymphomen der Haut. Von den solitären Lymphozytomen
treten zwei Drittel im Bereich des Kopfes auf, die bevorzugt
an Ohrläppchen, Brustwarze, Skrotum und Vulva lokalisiert
sind.
Der Schlüsselbericht zur Lyme-Neuroborreliose stammt von
Garin und Bujadoux aus dem Jahr 1922. Die Autoren beschreiben
den Krankheitsverlauf eines 58-jährigen Patienten, Schafzüchter
von Beruf, der nach einem Zeckenstich Mitte Juni 1922 ein markantes
Erythem entwickelte und dann etwa einen Monat später von
heftigen Schmerzen in Beinen, Rumpf und Arm befallen wurde,
begleitet von Lähmungen und Atrophie des rechten Deltamuskels.
Sein Gesundheitszustand verschlechterte sich und nahm schließlich
innerhalb von zweieinhalb Monaten einen Spontanverlauf mit Restdefekt,
einer Bewegungseinschränkung des rechten Armes. Der Bericht
ist retrospektiv die erste Schilderung des heute so genannten
Garin-Bujadoux-Bannwarth-Syndroms. Allerdings stellten die Autoren
noch keinen Zusammenhang mit dem Erythem her. Das erfolgte 1930
durch Sven Hellerström aus Stockholm, der über einen
Patienten berichtete, welcher drei Monate nach dem Auftreten
eines Erythema migrans eine Meningoenzephalitis entwickelte.
Im Jahr 1941 beschrieb Alfred Bannwarth aus München das
Syndrom einer
„Chronisch lymphozytären Meningitis mit dem klinischen
Bild der Neuralgie oder Neuritis“. Er unterschied Patienten
mit intensiven Nervenwurzelschmerzen, jüngere Patienten
mit Fazialislähmung und Patienten mit chronisch lymphozytärer
Meningitis mit zerebralen Symptomen wie starke Kopfschmerzen
und Erbrechen. Gemeinsam war allen Patienten ein entzündlicher
Liquor, eine lymphozytäre Pleozytose. Typisch für
diese Erkrankungen war auch, dass die heftigen Nervenschmerzen
besonders intensiv in der Nacht auftraten. Die Symptome dieser
Meningoradikuloneuritis schwanden erst nach Wochen oder Monaten.
Den kausalen Zusammenhang zwischen Zeckenstich, Erythema migrans
und Meningitis hat Bannwarth allerdings nicht erkannt, sondern
glaubte an einen rheumatisch-allergischen Ursprung.
Ausführlich studierten Schaltenbrand, Bammer & Schenk
und Hörstrup & Ackermann in den 1960er Jahren den klinischen
Verlauf und Liquor-Veränderungen bei Patienten mit dem
so genannten Bannwarth-Syndrom. Auf Hörstrup & Ackermann
geht die 1973 beschriebene und heute weiterhin aktuelle Bezeichnung
„Meningopolyneuritis Garin-Bujadoux-Bannwarth“ zurück.
Wolfgang Kristoferitsch aus Wien studierte in den späten
1970er und Anfang der 1980er Jahre ebenfalls sehr genau den
Krankheitsverlauf derartiger Patienten. Die von ihm erhobenen
Daten verwendete er dann, nach der Entdeckung der ursächlichen
Krankheitserreger, in kontrollierten Behandlungsstudien als
unbehandelte Kontrollgruppe, die den zeitlichen Ablauf im Spontanverlauf
repräsentierte. Die durchschnittliche Heilungsphase der
unbehandelten Lyme-Neuroborreliose beträgt etwa 25 Wochen
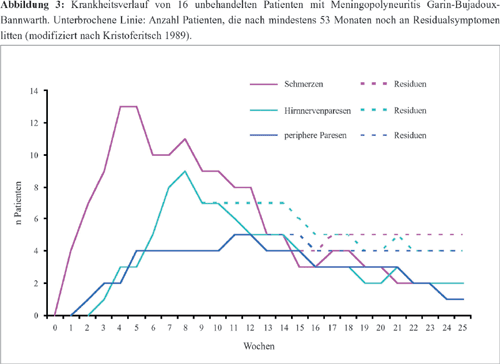
(Kristoferitsch 1989). Abbildung 3 zeigt eindrucksvoll, wie
die Schmerzsymptomatik bei der Meningopolyneuritis Garin-Bujadoux-Bannwarth
das Krankheitsbild beherrscht.
Als Penicillin nach dem Zweiten Weltkrieg in allgemeine Verwendung
kam, wurde es auch zur Behandlung der vorher genannten, zu dieser
Zeit noch idiopathischen Erkrankungen erprobt. 1949 berichtete
Niels Thyresson aus Stockholm von der sehr erfolgreichen Penicillin-Behandlung
von Patienten mit Acrodermatitis chronica atrophicans. Der therapeutische
Erfolg mit Penicillin machte nun klar, dass Bakterien eine ursächliche
Rolle spielen müssen. Über erfolgreiche Penicillin-Behandlung
von Patienten mit Erythema migrans berichtete Hollström
1951. Im Jahr 1974 beobachtete der Dermatologe Klaus Weber aus
München einen Patienten mit Erythema migrans, der trotz
erfolgreicher Behandlung der Hautläsion mit oralem Penicillin
eine Meningitis entwickelte. Die Meningitis wurde prompt mit
hohen Dosen von intravenösem Penicillin geheilt. Weber
folgerte, dass ein Bakterium für das Erythema migrans und
die damit verbundenen Erkrankungen verantwortlich sein muss.
Weber führte Ausschlussstudien durch, die auf serologischen
Testergebnissen beruhten und schloss Rickettsien, Francisellen
und andere Bakterien aus und diskutierte Borrelien als wahrscheinlichste
Möglichkeit. Weber, dem selbstverständlich wie den
anderen Forschern dieser Zeit die Überträgerrolle
von Ixodes-Zecken bestens bekannt war, hatte also das Rätsel
logisch gelöst. Allerdings stand der Überprüfung
ein Dogma der damaligen Akarologie im Weg, nämlich dass
Schildzecken keine Borrelien tragen.
|