| Periphere arterielle Verschlusskrankheit |
| E. Minar Univ.-Klinik für Innere Medizin II, Klin. Abteilung für Angiologie, Wien (Stv. Leiter: Univ.-Prof. Dr. E. Minar) |
|
Jeder sechste Diabetiker leidet an erheblichen Durchblutungsstörungen. Eine Makroangiopathie im Bereich der Extremitätenarterien bedeutet zugleich, dass die Lebensprognose dieser Patienten reduziert ist. Nach den Daten der Framingham-Studie beträgt die jährliche Inzidenz der peripheren Verschlusskrankheit bei männlichen Diabetikern in der Altersstufe zwischen 60 und 69 Jahren 16,3 bei Nichtdiabetikern hingegen 5,4. Die entsprechenden Inzidenzraten bei Frauen liegen bei 13,1 bzw. 3,1. Im Vergleich zum Nichtdiabetiker tritt beim Diabetiker die Gefäßkrankheit etwa 10 Jahre früher auf. Das Vorliegen einer Makroangiopathie im Bereich der Extremitätenarterien bedeutet gleichzeitig, dass die Lebensprognose dieser Patienten reduziert ist. Dies ist auf den meist vorliegenden Generalisationsgrad der atherosklerotischen Erkrankung zurückzuführen. Es konnte in mehreren epidemiologischen Studien gezeigt werden, dass die Dauer des NIDDM (nichtinsulinpflichtiger Diabetes mellitus) keinen Einfluss auf die kardiovaskuläre Morbidität und Mortalität hat. Der fehlende Einfluss der Diabetesdauer auf das Risiko kardiovaskulärer Komplikationen beim Typ-2-Diabetiker steht im Gegensatz zu der von der Diabetesdauer abhängigen Inzidenz makrovaskulärer Komplikationen beim Typ-1-Diabetiker. |
|
Makroangiopathie und diabetischer Fuß
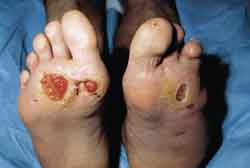
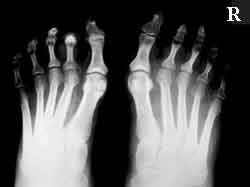
Aus therapeutischen und auch prognostischen Gründen ist es wichtig, zwischen ischämisch und neuropathisch verursachten Ulzera zu differenzieren, was meistens allein durch die klinische Untersuchung möglich ist. Für die beim Diabetiker gehäufte Amputationsrate ist in erster Linie der Schweregrad der Makroangiopathie verantwortlich, wobei insbesondere auch das Ausmaß der Begleitinfektion eine wesentliche Rolle spielt. Der Diabetiker ist zusätzlich gefährdet, durch die Entwicklung eines diabetischen Fußes auf Basis der Makroangiopathie beide Extremitäten zu verlieren. So ergibt sich bei 40% der Diabetiker mit Beinamputation im weiteren Krankheitsverlauf die Notwendigkeit der Amputation auch der kontralateralen Extremität. |
|
Diagnostisches Vorgehen bei PAVK Das diagnostische Vorgehen zur Abklärung einer Verschlusskrankheit unterscheidet sich beim Diabetiker prinzipiell nicht vom Nichtdiabetiker. Im Vordergrund steht die Anamnese und klinische Untersuchung des Patienten. Die Anamnese liefert beim Auftreten einer Claudicatio-Symptomatik bereits wesentliche Anhaltspunkte über die Verschlusslokalisation. Wegen der typischen, oft isolierten Beteiligung der Unterschenkelarterien werden öfters belastungsabhängige Schmerzen im Bereich der Fußsohle angegeben. Dem gegenüber tritt wegen der peripheren Verschlusslokalisation die Wadenclaudicatio als Leitsymptom im Gegensatz zur meist proximal lokalisierten Verschlusskrankheit des Nichtdiabetikers in den Hintergrund. Allerdings kann das klinische Bild der PAVK durch eine begleitende diabetische Polyneuropathie erheblich verfälscht werden. Der Verlust der Schmerzsensibilität kann die belastungsinduzierten ischämischen Wadenschmerzen und den Ruheschmerz verschleiern, womit diese alarmierenden Krankheitszeichen nicht wahrgenommen werden. Daher muss betont werden, dass gerade beim Diabetiker sehr häufig das Auftreten einer Gangrän die Erstmanifestation der Durchblutungsstörung darstellt, wobei der Patient vorher niemals an einer Claudicatio-Symptomatik gelitten hat. Die klinische Untersuchung des Diabetikers mit peripherer Verschlusskrankheit ist sicherlich die wichtigste diagnostische Maßnahme. Bei der Inspektion ist insbesondere auf kleinste akrale Läsionen zu achten, da diese oft rasch progredient zum Ausgangspunkt einer schweren Infektion werden können. Palpatorisch werden die typischen Pulslokalisationen untersucht, wobei beim Diabetiker insbesondere die Pulspalpation der Arteria poplitea für die Abschätzung der möglichen Therapiemaßnahmen von großer Bedeutung ist.
So liegt z.B. bei tastbarem Popliteapuls und fehlenden Fußpulsen eine Makroangiopathie vom Unterschenkeltyp vor, welche therapeutisch wegen der eingeschränkten Möglichkeiten einer lumeneröffnenden Therapie in diesem Bereich viel schwieriger zu beeinflussen ist als z.B. eine weiter proximal gelegene Verschlusskrankheit. Das Vorliegen einer Gangrän bei noch tastbaren Fußpulsen kann auf eine ganz periphere Makroangiopathie im Bereiche der Metatarsal- und Zehenarterien zurückzuführen sein bzw. auf einen thrombotischen Verschluss kleiner Gefäße im Rahmen einer Infektion.
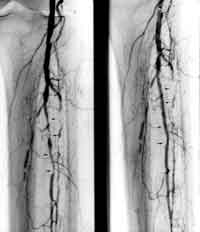
Zur weiteren Abklärung von Störungen im Bereich der Mikrozirkulation kommen spezielle Verfahren wie die Kapillarmikroskopie, die Laser-Doppler-Flussmessung sowie die transkutane Sauerstoffdruckmessung in Frage. Die Wahrscheinlichkeit für das Abheilen eines diabetischen Fußulkus kann durch die nichtinvasive apparativ-funktionelle Diagnostik gut abgeschätzt werden. In den letzten Jahren hat die (Farb-) Duplexsonographie die Angiographie für die primäre Lokalisationsdiagnose der Verschlusskrankheit zunehmend verdrängt. Allerdings ergeben sich gerade beim Diabetiker deutliche Einschränkungen dieser Methode. Darunter sind die eingeschränkte Beurteilbarkeit bei ausgedehnten Gefäßwandverkalkungen sowie die oft nur schwierige oder gar nicht mögliche morphologische Darstellung im Bereich der Unterschenkel- und Vorfußarterien zu erwähnen. Dies reduziert die Einsatzmöglichkeiten der Duplexsonographie beim Diabetiker, wo oft ausgedehnte Gefäßwandverkalkungen vorliegen und außerdem gerade die Unterschenkelarterien massiv betroffen sein können. Daher ist die Angiographie nach wie vor als diagnostischer Goldstandard der morphologischen Diagnostik der peripheren Verschlusskrankheit beim Diabetiker zu werten. Da es sich um eine invasive Untersuchung handelt, ist sie allerdings nur bei entsprechender Therapiekonsequenz indiziert. Vor der Kontrastmittelangiographie muss darauf geachtet werden, dass der Diabetiker ausreichend hydriert ist, um einer Beeinträchtigung der Nierenfunktion vorzubeugen.
In der letzten Zeit sind die Möglichkeiten und insbesondere auch die Verfügbarkeit der MR-Angiographie wesentlich verbessert worden, sodass in Hinkunft diese nichtinvasive Methode die invasive Kontrastmittelangiographie verdrängen wird. |
|
Therapie der PAVK beim Diabetiker Beeinflussung der Risikofaktoren Die Bedeutung einer Optimierung des Risikofaktorenprofils (insbesondere im Hinblick auf Fettstoffwechsel und Hypertonie) ist gut dokumentiert und soll hier nicht weiter diskutiert werden. Medikamentöse Sekundärprophylaxe Die günstige Beeinflussung kardiovaskulärer Komplikationen durch die Gabe von Thrombozytenfunktionshemmern konnte bei Patienten mit PAVK ausreichend dokumentiert werden. Es liegen jedoch nur sehr wenige Daten für Diabetiker vor. Die gerade bei Diabetikern gut dokumentierte gesteigerte Plättchenaktivität lässt jedoch auch bei diesen Patienten eine Wirksamkeit dieser Medikamente erwarten. Antikoagulantien kommen in der Sekundärprophylaxe nur bei speziellen Indikationen zur Anwendung, wobei insbesondere beim Diabetiker allfällige Kontraindikationen (z.B. proliferative Retinopathie) besonders beachtet werden müssen. Verbesserung der Symptomatik der Durchblutungsstörung Die Trainingstherapie stellt im Stadium II (Claudicatio intermittens) die Basis der Therapie dar. Als besonders günstige Voraussetzung für eine Verbesserung der schmerzfreien Gehstrecke ist der einseitige Ein-Etagen-Verschluss des Femoralis-Stromgebiets bei gleichzeitig nicht stenosierter Arteria profunda femoris als wichtigste Kollateralarterie anzusehen. Da jedoch gerade beim Diabetiker häufig auch ausgeprägte Veränderungen im Profunda-Stromgebiet vorliegen, muss die Möglichkeit einer fehlenden Besserung durch gleichzeitig vorliegende Profundastenosen in Betracht gezogen werden. Mehrere kontrollierte randomisierte Studien konnten für einige vasoaktive Substanzen nachweisen, dass sie die schmerzfreie Gehstrecke von Patienten mit Claudicatio intermittens im Vergleich zu Plazebo signifikant verbessern können. Allerdings wurden im Rahmen dieser Studien Diabetiker nicht als eigenes Kollektiv untersucht. Für die schweren klinischen Stadien III (ischämischer Ruheschmerz) und IV (Nekrose) konnte bisher keine klinische Wirksamkeit gesichert werden. Lediglich für die Substanzgruppe der Prostanoide (Prostaglandin E1; Iloprost®) ließ sich auch im klinischen Stadium III/IV nach Fontaine eine klinische Wirksamkeit dokumentieren. Es wurden auch Studien bei Diabetikern im Stadium III/IV durchgeführt, wobei ebenfalls eine klinische Wirksamkeit gesichert werden konnte. Lumeneröffnende Therapiemaßnahmen Bei den mit Amputationsgefährdung einhergehenden schweren Stadien der PAVK sollte, sofern irgendwie möglich, eine lumeneröffnende Therapiemaßnahme d.h. eine Beseitigung vorhandener Stenosen oder Verschlüsse angestrebt werden. Die modernen nichtchirurgischen Verfahren der Katheterrekanalisation (in erster Linie die PTA, perkutane transluminale Angioplastie) haben in den letzten Jahren einen wesentlichen Fortschritt gebracht und ermöglichen eine lumeneröffnende Therapie ohne wesentliche Belastung und Gefährdung des Patienten. Eine Katheterrekanalisation kann beim Diabetiker mit der gleichen Erfolgschance wie beim Nichtdiabetiker durchgeführt werden, allerdings sind die Langzeitergebnisse beim Diabetiker schlechter. Dies hängt einerseits mit dem rascheren Fortschreiten der Atherosklerose beim Diabetiker zusammen sowie andererseits mit der meist schlechten peripheren Ausstrombahn. Prinzipiell ist es allerdings auch möglich, Veränderungen im Bereich der Unterschenkelarterien mit speziellen Kathetertechniken zu behandeln (siehe Abbildung 1). Bei der Unmöglichkeit einer Katheter-Rekanalisation kommen gefäßchirurgische Eingriffe zur Anwendung. |
| Anschrift des Verfassers:
Univ.-Prof. Dr. Erich Minar Univ.-Klinik für Innere Medizin II, Klin. Abteilung für Angiologie A-1090 Wien, Währinger Gürtel 18-20 |