| Neuro-Osteoarthropathie |
| U. Dorn Landeskliniken Salzburg, Abteilung für Orthopädie (Vorstand: Prim. Univ.-Doz. Dr. U. Dorn) |
|
Diabetische periphere Neuropathie und damit einhergehende Veränderungen des knöchernen Fußskelettes werden unter dem Begriff der Neuro-Osteoarthropathie zusammengefasst. Die Kenntnisse über die Pathogenese skelettärer Alterationen sowie Veränderungen der Haut, Nerven, Gefäße und Muskeln der Füße diabetischer Patienten sind gerade in den letzten 10 Jahren entscheidend gewachsen. In früheren Publikationen wird fast ausnahmslos die periphere arterielle Verschlusskrankheit als Ursache trophischer Schäden an den Füßen von Diabetikern dargestellt. Zwangsläufig war damit in der Vergangenheit eine hohe Amputationsquote bei Diabetikern verbunden. Heute wissen wir, dass nur ein relativ kleiner Teil der Diabetiker mit Fußkomplikationen eine periphere arterielle Verschlusskrankheit aufweist, während bei dem größeren Teil dieser Patienten auf Grund der peripheren Neuropathie mit Weitstellung arterieller Gefäße sogar eine gesteigerte Durchblutung besteht. Diese diabetische periphere Neuropathie führt in weiterer Folge auch zu den charakteristischen Veränderungen des knöchernen Fußskelettes, die unter dem Begriff der Neuro-Osteoarthropathie zusammengefasst werden. Fasst man den Begriff diabetischer Fuß enger, so versteht man darunter eine Schädigung im Bereich der Füße als Folge eines Diabetes. Lange Zeit war damit das Bild der trockenen oder feuchten Gangrän assoziiert worden. Die komplexe Veränderung der Skelettarchitektur, die Dysbalance der Fußmuskulatur und der Ausfall wichtiger vegetativer Funktionen wie die der Schweißsekretion haben aber als gemeinsame Ursache die Neuropathie, ein Umstand, der lange Zeit nicht in unserem Wissen mit dem richtigen Stellenwert etabliert war. Auf Grund dieses fehlenden Wissens wurde die Prophylaxe vernachlässigt und erst der eingetretene Schaden behandelt. Dies führte in der Vergangenheit zu einer unnotwendig hohen Zahl an Amputationen.
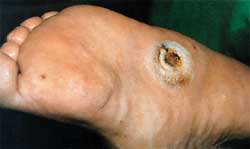
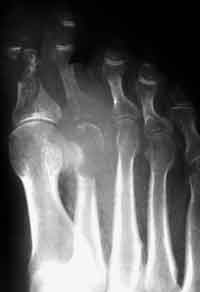
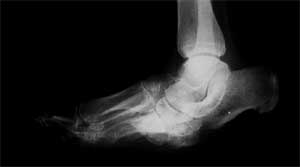
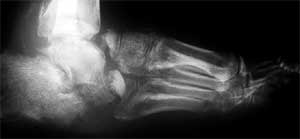
Durch Schädigung motorischer Nerven atrophieren insbesondere die kleinen Fußmuskeln und die Extensorenmuskulatur des Unterschenkels. Unelastischer Gang, Krallenzehenstellung und Überlastung der Mittelfußköpfchen sind direkte Folgen der motorischen Neuropathie. Die Schädigung der sensorischen Fasern bewirkt den Verlust der Schmerzempfindung, die Störung der Temperaturempfindung und die Verminderung der Tiefensensibilität. Häufige Hautverletzungen, Verbrennungen, Erfrierungen und Überbeanspruchung des Fußskelettes auf Grund mangelnder Bewegungskoordination sind die unmittelbaren Folgen. Das autonome Nervensystem reguliert die Durchblutung, Schweißsekretion und Hauttemperatur. Durch die Autosympathektomie kommt es zur Weitstellung peripherer Gefäße, genauer gesagt zur Öffnung arteriovenöser Shunts und damit zur Luxusperfusion, weiters zur Verminderung der Schweißsekretion. Diese beiden vegetativen Störungen führen dazu, dass der Fuß des Diabetikers meist auffällig warm und trocken ist. Die trockene, oft rissige Haut begünstigt als Eintrittspforte die Entstehung von Infektionen, zudem entstehen auf Grund verminderter mechanischer Eigenschaften über Knochenvorsprüngen Ulzerationen. Die diabetische Osteoarthropathie hat ihre Wurzeln ebenfalls in der Durchblutungsveränderung mit Öffnung arteriovenöser Shunts infolge der Schädigung des sympathischen Nervensystems. 0,15-2,5% der Diabetiker erkranken an der neuropathischen Osteoarthropathie. Infolge der gesteigerten Durchblutung kommt es durch resorptive Vorgänge zur Formveränderung des Fußskelettes mit verminderter mechanischer Belastbarkeit. Die Mittelfußknochen können das Aussehen abgelutschter Zuckerstangen annehmen. Da die Schutzfunktion der Oberflächen- und Tiefensensibilität reduziert ist, kommt es zur Überlastung der Fußwurzelknochen mit wiederkehrenden Mikro- und Makrofrakturen. Im Anschluss kommt es zu ausgedehnten und lange dauernden Umbauvorgängen des Fußskelettes. Subluxationen und Luxationen im Bereich des Chopart- und Lisfranc-Gelenkes führen zu massiven Deformitäten, wie vor allem der Knickplattfußdeformität bzw. zum typischen Schaukelfuß. Zur radiologischen Stadieneinteilung nach topographischen Gesichtspunkten eignet sich die Klassifikation von Sanders. Dabei werden 5 Typen unterschieden. Ca. 70% der Veränderungen entfallen auf Typ I, II und III. Nekrosen im Bereich der Metatarsophalangealgelenke werden als Typ I klassifiziert, daraus kann die Zuspitzung der Metatarsalia resultieren, die wiederum das Entstehen eines Ulkus begünstigt (siehe Abbildung 2). Bei Typ-II- Veränderungen (siehe Abbildung 3) sind hauptsächlich die Tarsometatarsalgelenke, also das Lisfranc-Gelenk betroffen. Durch Verformung der Cuneiformia entsteht nach Luxation des Naviculare der schwere Knick-Plattfuß. Der arthropathische Schaukelfuß entwickelt sich in Folge einer Nekrose vorwiegend im Bereich des Chopart-Gelenkes (= Typ III); siehe Abbildung 4. Der steil stehende Talus prädisponiert auf Grund der Drucküberlastung zur Entstehung des plantaren Ulkus im Fußwurzelbereich. Die seltenen Typ-IV-Veränderungen entsprechen Nekrosen im Bereich des oberen Sprunggelenkes bzw. des unteren Sprunggelenkes (= Typ V). Die verminderte Dämpfungseigenschaft des Fußskelettes führt in Kombination mit unzureichendem Schuhwerk oft nach kurzer Zeit zu ausgedehnter Ulzeration über druckbelasteten Knochenarealen und nachfolgend zur Infektion. Die häufigsten Mikroorganismen sind die gramnegativen aeroben Proteus mirabilis, Pseudomonas aeruginosa und E. coli sowie die grampositiven Enterokokken und Staphylococcus aureus.
Die Entstehung einer Ulzeration ist ein multifaktorielles Geschehen. Die Haut weist auf Grund der verminderten Schweißsekretion reduzierte mechanische Qualität auf, Schwielenbildung und Rissigkeit sind die Folge. Durch motorische Neuropathie entstehen Krallenzehen und der kontrakte Spreizfuß und damit überbelastete Hautareale. Besonders betroffen sind die Zehenkuppen, die Streckseite der Mittelgelenke und die Sohlenhaut über den Mittelfußköpfchen. Durch osteoarthropathische Deformierung des Fußskelettes entstehen zusätzlich überbeanspruchte Hautareale im Bereich der Fußwurzel und des Rückfußes. Durch die Formveränderung des Fußes wird die Mechanik der Muskeln und Sehnen beeinträchtigt, der daraus resultierende unelastische, plumpe Gang führt zu einem Anstieg von Druckbelastungen auf unphysiologische Werte. |
| Anschrift des Verfassers:
Prim Univ.-Doz. Dr. Ulrich Dorn LKH Salzburg, Abteilung für Orthopädie A-5020 Salzburg, Müllner Hauptstraße 48 |