| Bacillus anthracis: Speciesbestimmung und Subtypisierung mittels automatischer Ribotypisierung |
|
K. Grif 1, F. Allerberger 1, M.P.
Dierich 1, A. Wimmer 2, H. Plicka 2 |
| Schlüsselwörter:
Bacillus anthracis, Ribotypisierung, RiboPrinter® |
Zusammenfassung Fünf Bacillus anthracis-Isolate wurden mittels RiboPrinter® unter Verwendung von EcoRI, PvuII und AseI als Restriktionsenzyme ribotypisiert. Es handelte sich um drei Wildtypisolate von Anthrax-Fällen bei Rindern aus Tirol, um den Impfstamm Sterne 34F2 und ein im Dezember 2001 aus einem Postsack amerikanischer Diplomatenpost gewonnenes Isolat („Bundesheer-Stamm“). Als Kontrollstämme wurden Bacillus cereus DSM 345 und ein Bacillus megaterium-Blutkultur-Isolat verwendet. Mittels automatisierter Ribotypisierung unter Verwendung von EcoRI ist es möglich, nicht hämolysierende apathogene Bazillen von der B. anthracis/B.cereus-Gruppe zu differenzieren. Die Restriktionsenzyme AseI und PvuII erlauben zudem eine Subtypisierung verschiedener B. anthracis-Isolate. Die Bandenmuster der 3 Tiroler Wildtypisolate waren bei Verwendung von AseI und PvuII voneinander nicht unterscheidbar, jedoch im Bandenmuster klar different vom Sterne-34F2-Stamm und dem „Bundesheer-Stamm“. Das AseI-Bandenmuster der beiden letztgenannten Isolate differiert von dem für den Ames-Stamm publizierten Restriktionsmuster, was den „Bundesheer-Stamm“ von dem in den Vereinigten Staaten im Rahmen von Bioterrorismus eingesetzten Ames-Stamm abtrennt. Das Vorkommen von einzelnen Sporen von Bacillus anthracis als natürliche Kontamination ist in Geweben aus natürlichen Ursprungsmaterialen nicht ungewöhnlich. |
Key-words: Bacillus anthracis, ribotyping, RiboPrinter® |
Summary Using a RiboPrinter® with EcoRI, PvuII and AseI as restriction enzymes, five Bacillus anthracis-isolates were ribotyped. These are three wild type isolates from anthrax cases in cattle in the Tyrol, the vaccination strain Sterne 34F2 and an „Austrian army strain“ isolated from an American diplomatic postal bag in December 2001 in Vienna (Austria). Bacillus cereus DSM 345 and a Bacillus megaterium blood culture isolate were used as control strains. With automated ribotyping using EcoRI, it is possible to differentiate non-hemolytic apathogenic bacillae from the B. anthracis/B.cereus-group. In addition the restriction enzymes AseI and PvuII permit subtyping of different anthrax isolates. The band patterns of the three Tyrolean wild type isolates were indistinguishable from each other using AseI and PvuII but were, however, clearly different from the pattern of Sterne 34F2 and of the „Austrian army strain“. The AseI band patterns of both latter isolates differed from RiboPrinter® restriction patterns published for the Ames strain. This demonstrates that the „Austrian army strain“ is not identical to the Ames strain, allegedly used for bioterrorism in the United States during autumn 2001. It is not unusual for single spores of Bacillus anthracis to exist as natural contaminants in material fabrics of natural origins. |
| Einleitung
Wenngleich man über die tatsächliche Relevanz des Bedrohungspotentials Bioterrorismus und biologische Kriegsführung unterschiedlicher Meinung sein kann, sollte das öffentliche Gesundheitswesen auf die Erfordernisse schwerer Infektionskrankheiten vorbereitet sein [1]. Am 4. Oktober 2001 wurde in Florida bei einem 63-jährigen Patienten Lungenmilzbrand festgestellt [2]. Da auch bei einem Arbeitskollegen und am Arbeitsplatz (America Media Incorporated, Boca Raton, Florida) des letztendlich Verstorbenen Bacillus anthracis nachgewiesen wurde, war von einem beabsichtigten Ausbringen von Sporen auszugehen. Am 12. Oktober 2001 wurde Hautmilzbrand bei einem Angestellen des Medienkonzerns ABS in New York festgestellt [3]. Wegen einer Hautläsion hatte er initial einen Infektiologen aufgesucht, welcher die Verdachtsdiagnose stellte. Die kulturelle Verifizierung der Diagnose wurde im Hinblick darauf, dass auch hier von einer absichtlichen Ausbringung von Milzbrandsporen auszugehen ist, behördlich bestätigt. Mit diesen Fällen wurde leider bewiesen, dass Bioterrorismus als mögliches Szenario grundsätzlich zu bedenken ist. Der Charakterisierung von B. anthracis-Isolaten zur Gewinnung von Rückschlüssen über die Herkunft der Bakterien kommt deshalb große Bedeutung zu. Wir beschreiben die Eignung von automatischer Ribotypisierung als Mittel zur Speciesidentifizierung und Subtypisierung bei B. anthracis. |
| Material
und Methoden
Bakterienisolate Ribotypisierung |
| Ergebnisse
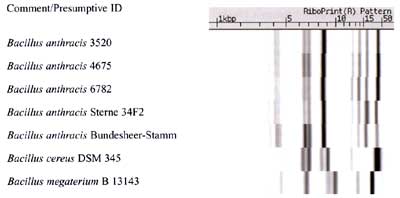
Abbildung 1 gibt die Ergebnisse der
Ribotypisierung unter Verwendung von EcoRI als Restriktionsenzym
wieder. Der automatische Vergleich der gewonnenen Banden-Muster
mit Mustern in der Qualicon®-Datenbank erbrachte für das
B. megaterium-Isolat B13143 eine korrekte Species-Diagnose.
Die fünf B. anthracis-Isolate erbrachten ein einheitliches
Bandenmuster, welches vom Gerät als B. cereus-Muster
eingestuft wurde.
Abbildung 2 gibt die Ergebnisse der
Ribotypisierung unter Verwendung von AseI als Restriktionsenzym
wieder. Für das Genus Bacillus steht für dieses
Restriktionsenzym derzeit keine Datenbank zur Verfügung. B.
cereus DSM345 und B. megaterium B13143 erbrachten eigenständige,
voneinander und von Bacillus anthracis zu unterscheidene
Bandenmuster. Innerhalb der B. anthracis-Gruppe zeigten die
drei Tiroler Isolate idente, charakteristische und von den zwei
verbleibenden B. anthracis-Isolaten unterschiedliche Bandenmuster.
Abbildung 3 gibt die Ergebnisse der
Ribotypisierung unter Verwendung von PvuII als Restriktionsenzym
wieder. Für das Genus Bacillus steht für dieses
Restriktionsenzym derzeit keine Datenbank zur Verfügung. B.
cereus DSM345 und B. megaterium B13143 erbrachten eigenständige,
voneinander und von B. anthracis zu unterscheidende Bandenmuster.
Innerhalb der B. anthracis-Gruppe zeigten die drei Tiroler
Isolate idente, charakteristische und von den zwei verbleibenden
Anthrax-Isolaten unterschiedliche Bandenmuster.
|
| Diskussion
Bacillus anthracis ist eine genetisch sehr uniforme Bakterienspecies mit erstaunlich geringer Variabilität [7], was zwar molekulare Diagnostik erleichtert, eine Subtypisierung zur Gewinnung epidemiologischer Rückschlüsse jedoch erschwert. Phänotypisch lassen sich Isolate selbst unterschiedlichster geographischer Herkunft nicht differenzieren [8]. Die biochemischen und serologischen Methoden, die bei anderen Pathogenen zur Subtypisierung zum Einsatz kommen, haben, ebenso wie die Phagentypisierung, bei B. anthracis keinen Wert. Turnbull et al. postulierten, dass dieser exzeptionelle Species-Monomorphismus auf – im Vergleich zu allen anderen Species – relativ geringe Anzahl von Vermehrungszyklen zurückzuführen ist [8]. Vermehrungszyklen von B. anthracis hängen weitgehend von Tierinfektionen ab, wobei beträchtliche Zeitintervalle zwischen solchen Vorfällen liegen können. Da die Vermehrung praktisch ausschließlich im Tierkörper stattfindet, seien Vegetativformen von B. anthracis nur selten „Mutagenen, Phagen oder anderen Umwelteinflüssen, die Stammvariationen bewirken können“, ausgesetzt [8]. Somit bleiben bei dieser monomorphen Spezies lediglich molekulargenetische Subtypisierungsverfahren, welche in den letzten Jahren zunehmend verfeinert wurden [9, 10, 11, 12, 13]. Molekulargenetische Typisierungsverfahren, die auf der Variabilität der Anzahl von „tandem repeats“ in der variablen Region des vrrA-Gens basieren, gelten derzeit als Goldstandard: Sie gestatten es, alle derart getesteten Stämme dieser genetisch monomorphen Bakterienart in fünf Kategorien einzuordnen und somit Hinweise auf die jeweilige Herkunft von B. anthracis-Isolaten zu geben [14, 15]. Mittels automatisierter Ribotypisierung
unter Verwendung von EcoRI ist es möglich, nicht hämolysierende
Bazillen von der B. anthracis/B.cereus-Gruppe zu differenzieren
[5]. Die Restriktionsenzyme AseI und PvuII erlauben
zudem eine Subtypisierung verschiedener Anthrax-Isolate. Die publizierten
Sequenzen der 16S und 23S rRNA-Gene von B. anthracis und
B. cereus enthalten keine „restriction sites“ für
AseI. Die 4 bis 5 Banden, alle über 5 kbp (Abbildung
3) reflektieren somit die Platzierung der ribosomalen Operons im
Bacillus-Chromosom. AseI-Ribotypisierung bietet sich
somit für eine erste Subtypisierung von B. anthracis
an. Auch für PvuII enthalten die publizierten Sequenzen
der 16S und 23S rRNA-Gene von B. anthracis und B. cereus
keine Restriktionsstellen. Zudem sind die generierten Bandenmuster
mit 10 Banden komplexer als die Muster von AseI, was die
Verwendung von PvuII im Anschluss an die Subtypisierung mit
AseI anbietet. Der Ausschluss der Species B. anthracis ist in der Veterinärmedizin und der Humanmedizin vor allem bei nicht-hämolysierenden Bacillus-Blutkulturisolaten erforderlich [19, 20]. Unsere Ergebnisse unterstreichen das beachtliche Potential von automatischer Ribotypisierung, welche im Bedarfsfall binnen weniger Stunden derartige Speciesbestimmungen ermöglicht. Zudem erlaubt die Ribotypisierung eine Subtypisierung von B. anthracis und somit epidemiologische Rückschlüsse über die Herkunft von Isolaten. |
| Literatur:
1. Allerberger F.: „Pest-Milzbrand-Tularämie.“ Antibiotika Monitor tom. XVII, 3/4 (1998) 4. 2. Bush L.M., Abrams B.H., Beall A., Johnson C.C.: „Index case of fatal inhalation anthrax due to Bioterrorism in the United States.“ N. Engl. J. Med. 345 (2001) 1607-1626. 3. Centers for Disease Control
and Prevention (CDC). Update: public health message regarding anthrax.
12 October 2001 (htp://www.bt.cdc.gov/DocumentApp/Anthrax/ 4. Khaschabi D., Schönbauer M.: „Mikrobiologische Diagnostik von Milzbrand.“ Antibiotika Monitor tom. XIV, 3/4 (1998) 55-60. 5. Huemer H.P., Grif K., Allerberger F., Rotter M.: „Diagnostik und Typisierung von Bacillus anthracis mittels Rapid-PCR und Ribotyping.“ Antibiotika Monitor tom. XIV, 5/6 (2001) 105-108. 6. Grif K., Karch H., Schneider C., Daschner F., Beutin L., Cheasty T., Rowe B., Dierich M.P., Allerberger F.: „Comparative study of five different techniques for epidemiological typing of Escherichia coli O157.“ Diag. Microbiol. Infect. Dis. 32 (1998) 165-176. 7. Keim P., Kalif A., Schupp J., Hill K., Travis S.E., Richmond K., Adair D.M., Hugh-Jones M., Kuske C.R., Jackson P.: „Molecular evolution and diversity in Bacillus anthracis as detected by amplified fragment length polymorphism markers.“ J. Bacteriol. 179 (1997) 818-824. 8. Turnbull P.C.B.: „Guidelines for the Surveillance and Control of Anthrax in Humans and Animals.“ 3rd edition. WHO/EMZ/ZDI/98.6. (http://www.who.int/emc) 9. Henderson I.: „Fingerprinting Bacillus anthracis strains.“ Salisbury Med. Bull. 87, special suppl. (1996) 55-58. 10. Anderson G.L., Simchock J.M., Wilson K.H.: „Identification of a region of genetic variability among Bacillus anthracis strains and related species.“ J. Bacteriol. 178 (1996) 377-384. 11. Kaim P., Kalif A.S, Schupp J., et al.: „Molecular evolution and diversity of Bacillus anthracis as detected by amplified fragment length polymorphism markers.“ J. Bacteriol. 179 (1997) 818-824. 12. Jackson P.J., Walthers A., Kalif A.S., et al.: „Characterization of the variable-number tandem repeats in vrrA from different Bacillus anthracis isolates.“ Appl. Environ. Microbiol. 63 (1997) 1400-1405. 13. Jackson P.J., Hugh-Jones M.E., Adair D.M., Green G., Hill K.K., Kuske C.R., Grinberg L.M., Abramova F.A., Keim P.: „PCR analysis of tissue samples from the 1979 Sverdlosk anthrax victims: the presence of multiple Bacillus anthracis strains in different victims.“ Proc. Natl. Acad. Sci. USA 95 (1998) 1224-1229. 14. Swartz M.: (2001) „Recognition and management of anthrax – an update.“ N. Engl. J. Med. 345 (2001) 1621-1625. 15. Keim P., Smith K.L., Keys C., Takahashi H., Kurata T., Kaufmann A.: „Molecular investigation of the Aum Shinrikyo anthrax release in Kameido, Japan.“ J. Clin. Microbiol. 39 (2001) 4566-4567. 16. Stroman D.W., McLeyan C, Rogers J.: „Discrimination between B. anthracis, B. cereus, B. mycoides and B. thuringiensis strains by automated rRNA operon ribotyping.“ Abstracts of the 98th general meeting of the American Society for Microbiology, ASM, Washington DC (1998) 2005-4171. 17. RiboPrint® pattern provided by Joel B. Hansen. 18. Pfisterer R.M.: „Epidemiologie und Klinik des Milzbrandes.“ Antibiotika Monitor tom. XIV, 3/4 (1998) 48-54. 19. Greenberg D.S.: „War, bioterrorism and the political landscape.“ Lancet 358 (2001) 2137. 20. Anonymus: „Interim European surveillance case definition for anthrax.“ Eurosurveillance Weekly 5: 011101 (2001). (http://www.eurosurv.org/2001/011101.htm) |
|
Anschrift des
Verfassers:
|